Nhiệt phân hoàn toàn 27,3 g một hỗn hợp rắn X gồm NaNO3 và Cu(NO3)2
Bài 9: Axit nitric và muối nitrat
Giải bài 14 trang 16 SBT Hóa 11 Bài 9: Axit nitric và muối nitrat giúp học sinh biết cách làm bài tập trong SBT Hóa 11.
Bài 9.14 trang 16 Sách bài tập Hóa học 11: Nhiệt phân hoàn toàn 27,3 g một hỗn hợp rắn X gồm NaNO3 và Cu(NO3)2, thu được hỗn hợp khí có thể tích 6,72 lít (đktc).
1. Viết phương trình hoá học của các phản ứng xảy ra.
2. Tính thành phần % về khối lượng của mỗi muối trong hỗn hợp X.
Lời giải:
1. Phương trình hoá học của các phản ứng:
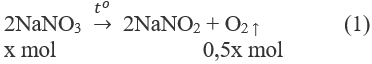
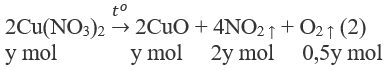
2. Đặt X và y là số mol của NaNO3 và Cu(NO3)2 trong hỗn hợp X. Theo các phản ứng (1) và (2) số mol NO2 thu được là 2y mol và tổng số mol oxi là (0,5x + 0,5y) mol.
Biết khối lượng mol của hai chất NaNO3 và Cu(NO3)2 tương ứng là 85 và 188 (g/mol), ta có hệ phương trình :
85x + 188y = 27,3 (a)
0,5x + 2y + 0,5y = 0,3 (b)
Giải hệ phương trình (a), (b) được : x = y = 0,1.
Phần trăm khối lượng của mỗi muối trong hỗn hợp X :
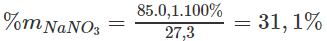
%mCu(NO3)2 = 100% - 31,1% = 68,9%

