Một bình kín dung tích 8,4 lít có chứa 4,96 g 02 và 1,3 gam hỗn hợp khí A gồm 2 hiđrocacbon
Bài 33: Luyện tập: Ankin
Giải bài 7 trang 52 SBT Hóa 11 Bài 33: Luyện tập: Ankin giúp học sinh biết cách làm bài tập trong SBT Hóa 11.
Bài 33.7 trang 52 Sách bài tập Hóa học 11: Một bình kín dung tích 8,4 lít có chứa 4,96 g 02 và 1,3 gam hỗn hợp khí A gồm 2 hiđrocacbon. Nhiệt độ trong bình t1 = 0oC và áp suất trong bình p1 = 0,5 atm.
Bật tia lửa điện trong bình kín đó thì hỗn hợp A cháy hoàn toàn. Sau phản ứng, nhiệt độ trong bình là t2 = 136,5oC và áp suất là p2 atm. Dẫn các chất trong bình sau phản ứng đi qua bình thứ nhất đựng H2SO4 đặc, sau đó qua bình 2 đựng dung dịch NaOH (có dư) thì khối lượng bình thứ hai tăng 4,18 g.
1. Tính p2, biết rằng thể tích bình không đổi.
2. Xác định công thức phân tử và phần trăm theo thể tích của từng chất trong hỗn hợp A nếu biết thêm rằng trong hỗn hợp đó có một chất là anken và một chất là ankin.
Lời giải:
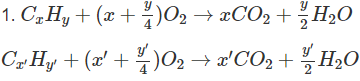
H2SO4 + nH2O → H2SO4.nH2O
2NaOH + CO2 → Na2CO3 + H2O
Số mol CO2 là:
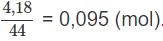
Khối lượng C trong hỗn hợp A là: 0,095.12 = 1,14 (g).
Khối lượng H trong hỗn hợp A là: 1,3 - 1,14 = 0,16 (g).
Số mol H2O sau phản ứng là:
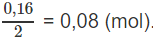
Để tạo ra 0,095 mol CO2 cần 0,095 mol O2;
Để tạo ra 0,08 mol H2O cần 0,04 (mol) O2.
Số mol O2 đã tham gia phản ứng là: 0,095 + 0,04 = 0,135 (mol).
Số mol O2 ban đầu là:
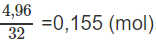
Số mol O2 còn dư là: 0,155 - 0,135 = 0,02 (mol).
Số mol 3 chất trong bình sau phản ứng:
0,095 + 0,08 + 0,02 = 0,195 (mol).
Nếu ở đktc thì Vo = 0,195.22,4 = 4,37 (lít).
Thực tế V2 = 8,4 lít
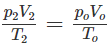
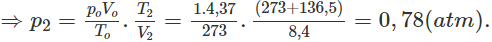
2. Đổi thể tích hỗn hợp khí trước phản ứng về đktc:
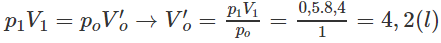
Số mol khí trước phản ứng:
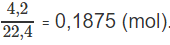
Số mol 2 hiđrocacbon: 0,1875 - 0,155 = 0,0325 (mol).
Đặt lượng CnH2n là a mol, lượng CmH2m-2 là b mol, ta có a + b = 0,0325.
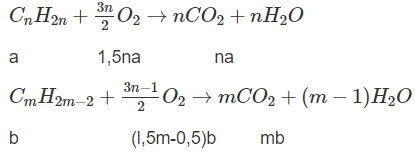
Số mol O2: l,5na + (l,5m - 0,5)b = 0,135 (2)
Số mol CO2: na + mb = 0,095 (3)
Từ (2) và (3), tìm được b = 0,015 ⇒ a = 0,0175
Thay các giá trị của a và b vào (3), ta có :
1,75.10−2n + 1,5.10−2m = 9,5.10−2
7n + 6m = 38
Nếu n = 2 thì
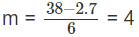
Nếu n = 3 thì
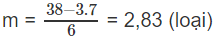
Nếu n > 3 thì m < 2 (loại).
% về thể tích của C2H4:

% về thể tích của C4H6 là 46,2%

