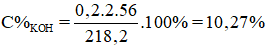Điện phân 200 ml dung dịch KOH 2M (D = 1,1 g/cm3) với điện cực trơ
SBT Hóa học 12 Bài 21: Điều chế kim loại
Giải bài 4 trang 46 SBT Hóa học 12 chi tiết trong bài học Bài 21: Điều chế kim loại giúp học sinh biết cách làm bài tập Hóa 12.
Bài 21.4 trang 46 Sách bài tập Hóa học 12: Điện phân 200 ml dung dịch KOH 2M (D = 1,1 g/cm3) với điện cực trơ. Khi ở catot thoát ra 2,24 lít khí (đktc) thì ngừng điện phân. Biết rặng nước bay hơi không đáng kể. Dung dịch sau điện phân có nồng độ phần trăm là
A. 10,27%. B. 10,18%.
C. 10,9%. D. 38,09%.
Lời giải:
A
Khi điện phân:
(K): 2H2O + 2e → 2OH- + H2
nH2 = 0,1 mol ⇒ ne nhận = 0,2 mol
(A): 2H2O → 4H+ + O2 + 4e
Bảo toàn e ta có: ne cho = n e nhận = 0,2 mol
nO2 = ¼ n e cho = 0,05 mol
mdung dịch sau phản ứng = mdd ban đầu – mO2 – mH2 = 200.1,1 – 0,1.2 – 0,05.32 = 218,2g