Cho phản ứng đơn giản có dạng: aA + bB suy ra cC + dD. Mối quan hệ giữa nồng độ và tốc độ tức thời
Câu hỏi:
Cho phản ứng đơn giản có dạng: aA + bB ⟶ cC + dD
Mối quan hệ giữa nồng độ và tốc độ tức thời của phản ứng hóa học được biểu diễn bằng biểu thức
A. 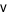 =
= 
B. 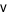 =
= 
C. 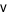 =
= 
D. 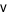 =
= 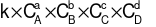
Trả lời:
Đáp án đúng là: A
Cho phản ứng đơn giản có dạng: aA + bB ⟶ cC + dD
Theo định luật tác dụng khối lượng, mối quan hệ giữa nồng độ và tốc độ tức thời của phản ứng hóa học được biểu diễn bằng biểu thức 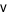 =
= 
Trong đó, k là hằng số tốc độ phản ứng; CA, CB là nồng độ (M) chất A, chất B tại thời điểm đang xét.
Xem thêm bài tập trắc nghiệm Hóa 10 CTST có lời giải hay khác:
Câu 3:
Biểu thức tốc độ trung bình của phản ứng: aA + bB ⟶ cC + dD là
Xem lời giải »
Câu 4:
Cho phản ứng ở 45°C
2N2O5 (g) ⟶ O2 (g) + 2N2O4 (g)
Sau 275 giây đầu tiên, nồng độ của O2 là 0,188 M. Tính tốc độ trung bình của phản ứng theo O2 trong khoảng thời gian trên.
Xem lời giải »
Câu 5:
Cho phản ứng: 2SO2 (g) + O2 (g) 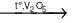 2SO3 (g)
2SO3 (g)
Biểu thức tốc độ thức thời của phản ứng theo định luật tác dụng khối lượng là
Xem lời giải »
Câu 7:
Hằng số tốc độ phản ứng k bằng vận tốc tức thời 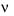 khi
khi
Xem lời giải »
Câu 8:
Cho phản ứng đơn giản xảy ra trong bình kín: 2CO (g) + O2 (g) ⟶ 2CO2 (g).
Tốc độ phản ứng thay đổi như thế nào nếu tăng nồng độ CO gấp 2 lần, nồng độ O2 không đổi.
Xem lời giải »
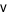 =
= 
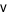 =
= 
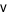 =
= 
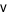 =
= 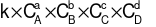
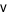 =
= 

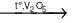 2SO3 (g)
2SO3 (g)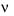 khi
khi