Tính pH của các dung dịch sau Dung dịch NaOH 0,1 M Dung dịch HCl 0,1 M
Tính pH của các dung dịch sau: --> --> --> -->
Giải Hóa 11 Bài 3: Ôn tập chương 1 - Kết nối tri thức
Câu hỏi 3 trang 28 Hóa học 11: Tính pH của các dung dịch sau:
a) Dung dịch NaOH 0,1 M;
b) Dung dịch HCl 0,1 M;
c) Dung dịch Ca(OH)2 0,01 M.
Lời giải:
a) NaOH → Na+ + OH-
0,1 → 0,1 M
Ta có: [H+].[OH]- = 10-14
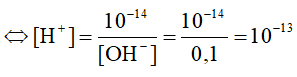
Ta có: pH = -log[H+] = 13.
b) HCl → H+ + Cl-
0,1 → 0,1 M
Ta có: pH = -log[H+] = 1 M.
c) Ca(OH)2 → Ca2+ + 2OH-
0,01 → 0,02 M
Ta có: [H+].[OH]- = 10-14
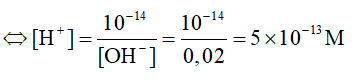
Ta có: pH = -log[H+] = 12,3.
Lời giải Hóa 11 Bài 3: Ôn tập chương 1 Kết nối tri thức hay khác:

