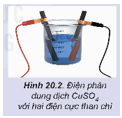
Quan sát Hình 20.2 và thực hiện các yêu cầu sau trang 96 Hóa học 12
Quan sát Hình 20.2 và thực hiện các yêu cầu sau:
Giải Hóa 12 Bài 20: Kim loại trong tự nhiên và phương pháp tách kim loại - Kết nối tri thức
Hoạt động trang 96 Hóa học 12: Quan sát Hình 20.2 và thực hiện các yêu cầu sau:
1. Cho biết điện cực nào là điện cực dương, điện cực nào là cực âm.
2. Hãy viết các phương trình xảy ra trên các điện cực và phương trình hoá học của phản ứng điện phân dung dịch CuSO4.
Lời giải:
1. Điện cực gắn với dây màu đỏ là anode (cực dương); điện cực gắn với dây màu đen là cathode (cực âm) do có lớp kim loại bám ngoài điện cực.
2.
+ Ở anode có thể xảy ra sự oxi hoá ion sulfate hoặc phân tử H2O. Tuy nhiên, vì H2O dễ bị oxi hoá hơn ion sulfate nên H2O bị oxi hoá trước, tạo thành sản phẩm là khí O2.
+ Ở cathode có thể xảy ra sự khử ion Cu2+ hoặc phân tử H2O. Vì ion Cu2+ dễ bị khử hơn H2O nên ion Cu2+ bị khử trước, tạo thành ion kim loại Cu bám trên cathode.
Phương trình hoá học của phản ứng điện phân dung dịch CuSO4:
2CuSO4 + 2H2O 2Cu + O2 + 2H2SO4
(Lưu ý: Thường coi ion không bị điện phân)
Lời giải Hóa 12 Bài 20: Kim loại trong tự nhiên và phương pháp tách kim loại hay khác: