Chọn nguyên tố thể hiện tính kim loại nhiều hơn trong mỗi cặp nguyên tố sau
Giải SBT Hóa học 10 Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
Haylamdo biên soạn và sưu tầm lời giải Bài 7.6 trang 21 sách bài tập Hóa học 10 trong Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm sách Cánh diều. Với lời giải chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập trong SBT Hóa học 10.
Bài 7.6 trang 21 sách bài tập Hóa học 10: Chọn nguyên tố thể hiện tính kim loại nhiều hơn trong mỗi cặp nguyên tố sau:
a) Sr và Sb.
b) As và Bi.
c) B và O.
d) S và As.
Lời giải:
a) Sr và Sb.
Sr và Sb cùng thuộc chu kì 5, ZSr < ZSb nên Sr thể hiện tính kim loại nhiều hơn so với Sb.
b) As và Bi.
As và Bi cùng thuộc nhóm VA, ZAs < ZBi nên Bi thể hiện tính kim loại nhiều hơn so với As.
c) B và O.
B và O cùng thuộc chu kì 2, ZB < ZO nên B thể hiện tính kim loại nhiều hơn so với O.
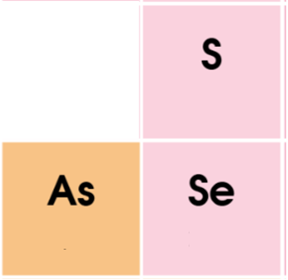
d) S và As.
So sánh gián tiếp thông qua Se.
Tính kim loại: As > Se > S
Vậy As thể hiện tính kim loại nhiều hơn S.