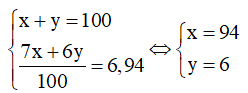Tính thành phần phần trăm của mỗi đồng vị lithium trong tự nhiên
Giải SBT Hóa 10 Ôn tập chương 1
Haylamdo biên soạn và sưu tầm lời giải Bài OT 1.7 trang 17 trong Ôn tập chương 1 sách Chân trời sáng tạo. Với lời giải chi tiết nhất hy vọng sẽ giúp học sinh dễ dàng nắm được cách làm bài tập Sách bài tập Hóa 10.
Bài OT 1.7 trang 17 SBT Hóa học 10: Lithium trong tự nhiên có 2 đồng vị là và . Nguyên tử khối trung bình của lithium là 6,94. Tính thành phần phần trăm của mỗi đồng vị lithium trong tự nhiên.
Lời giải:
Gọi % số nguyên tử của mỗi đồng vị và lần lượt là x và y.
Theo bài ra, ta có hệ phương trình:
Vậy % số nguyên tử của mỗi đồng vị và lần lượt là 94% và 6%.