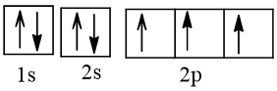
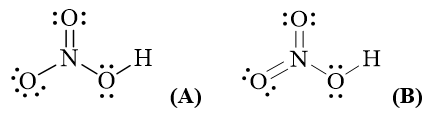Viết cấu hình electron của nguyên tử nitrogen (7N) theo ô orbital
Sách bài tập Hóa học 11 Bài 5: Một số hợp chất quan trọng của nitrogen - Cánh diều
Bài 5.8 trang 19 Sách bài tập Hóa học 11: a)Viết cấu hình electron của nguyên tử nitrogen (7N) theo ô orbital. Nguyên tử N có bao nhiêu electron hoá trị ghép đôi, bao nhiêu electron hoá trị độc thân?
|
b) Có 2 đề xuất về công thức Lewis của phân tử HNO3 như bên: |
|
b1) Công thức (A) hay (B) phù hợp với đặc điểm các electron hoá trị của nguyên tử nitrogen? Theo công thức đó, hoá trị và số oxi hoá của N là bao nhiêu?
b2*) Kết quả nghiên cứu cho biết giá trị độ dài các liên kết giữa nguyên tử N và O (liên kết NO) trong phân tử HNO3 là 1,406 Å; 1,211 Å và 1,199 Å. Công thức (A) hay (B) có thể thoả mãn các số liệu đã cho? Giải thích.
Lời giải:
a) Cấu hình electron của nitrogen theo ô orbital:
Có 1 cặp electron hoá trị ghép đôi, 3 electron hoá trị độc thân.
b)
b1)Công thức (A) phù hợp hơn vì nguyên tử N chỉ có 4 orbital hoá trị, do đó chỉ có thể tạo tối đa 4 liên kết cộng hoá trị. Theo công thức (A), N có hoá trị là IV và số oxi hoá là +5.
b2*) Công thức (A) phù hợp với dữ liệu do có ba loại liên kết giữa N và O không tương đương nhau trong phân tử HNO3 (1 liên kết đôi, 1 liên kết đơn theo kiểu ghép đôi electron hoá trị và 1 liên kết đơn theo kiểu cho - nhận).
Lời giải SBT Hóa 11 Bài 5: Một số hợp chất quan trọng của nitrogen hay khác: