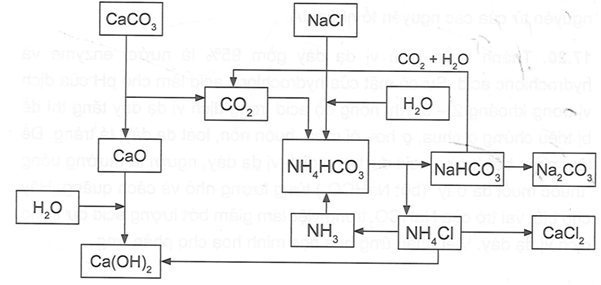
Sơ đồ dưới đây mô tả quá trình Solvay để điều chế Na2CO3 trong công nghiệp
Sách bài tập Hóa học 12 Bài 17: Nguyên tố nhóm IA - Chân trời sáng tạo
Câu 17.16 trang 111 Sách bài tập Hóa học 12: Sơ đồ dưới đây mô tả quá trình Solvay để điều chế Na2CO3 trong công nghiệp.
Dựa vào sơ đồ trên, hãy:
a. Viết phương trình của phản ứng tổng quát tạo Na2CO3.
b. Viết phương trình cân bằng của cặp muối NaCl/ NH4HCO3.
c. Viết phương trình hình thành NH4HCO3.
d. Nêu vai trò của Ca(OH)2 trong quá trình và viết phương trình phản ứng.
Lời giải:
a. Phương trình hóa học tổng quát tạo Na2CO3:
- Nung CaCO3 ở 950 – 1100oC, dẫn khí thoát ra vào dung dịch bão hòa NaCl trong NH3:
CaCO3 CaO + CO2
NaCl + NH3 + CO2 + H2O → NaHCO3 + NH4Cl
Tách NaHCO3 ra khỏi dung dịch, nung ở nhiệt độ 450oC – 500oC thu được soda:
2NaHCO3 Na2CO3 + CO2 + H2O
b. Phương trình cân bằng của cặp muối NaCl/ NH4HCO3
NaCl + NH4HCO3 ⇌ NaHCO3 + NH4Cl
c. Viết phương trình tạo thành NH4HCO3:
2NH3 + CO2 + H2O → (NH4)2CO3
(NH4)2CO3 + CO2 + H2O → 2NH4HCO3
d. Sản phẩm NH4Cl chế hóa với vôi tôi thu khí NH3:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O
Các khí CO2, NH3 được đưa vào sử dụng lại. NH3 được tuần hoàn trong quá trình sản xuất, do đó phương pháp Solvay còn được gọi là phương pháp tuần hoàn ammonia.
Lời giải SBT Hóa 12 Bài 17: Nguyên tố nhóm IA hay khác:
Câu 17.1 trang 108 Sách bài tập Hóa học 12: Nguyên tử của các nguyên tố nhóm IA khác nhau về ....
Câu 17.5 trang 108 Sách bài tập Hóa học 12: Cho các dãy kim loại sau: Fe, Na, K, Cu và Li ....
Câu 17.6 trang 109 Sách bài tập Hóa học 12: Nước Javel là sản phẩm của quá trình ....
Câu 17.7 trang 109 Sách bài tập Hóa học 12: Phương pháp điều chế NaOH trong công nghiệp là ....
Câu 17.8 trang 109 Sách bài tập Hóa học 12: Cho sơ đồ phản ứng: NaCl → X → NaHCO3 → Y → NaNO3 ....
Câu 17.9 trang 109 Sách bài tập Hóa học 12: Cho a mol CO2 vào dung dịch chứa b mol NaOH ....
Câu 17.10 trang 110 Sách bài tập Hóa học 12: Cho 0,53 gam muối carbonate của kim loại nhóm IA ....
Câu 17.11 trang 110 Sách bài tập Hóa học 12: Để xác định 3 hợp chất X, Y, Z đều là muối của Na ....