Giải Chuyên đề Hóa học 10 trang 32 Cánh diều
Haylamdo biên soạn và sưu tầm lời Giải Chuyên đề Hóa học 10 trang 32 trong Bài 4: Entropy và biến thiên năng lượng tự do Gibbs sách Cánh diều. Với lời giải hay nhất, chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập Chuyên đề Hóa 10.
Chuyên đề Hóa học 10 trang 32 Cánh diều
Bài tập 1 trang 32 Chuyên đề học tập hóa học 10: Thả một vài tinh thể patassium dichromate K2Cr2O7 màu cam đỏ vào nước (Hình 4.3). Entropy của quá trình hòa tan này tăng hay giảm? Giải thích.
Lời giải:
Thả một vài tinh thể patassium dichromate K2Cr2O7 màu cam đỏ vào nước, tinh thể patassium dichromate K2Cr2O7 tan trong nước ⇒ Độ mất trật tự của các ion trong tinh thể tăng ⇒ Entropy của quá trình hòa tan này tăng.
Bài tập 2 trang 32 Chuyên đề học tập hóa học 10: Hãy đánh giá khả năng tự xảy ra của phản ứng sau ở nhiệt độ chuẩn:
2Al(s) + 3H2O(l) → Al2O3(s) + 3H2(g)
Biết rằng: = - 818,3 kJ, được tính theo số liệu cho trong Phụ lục 1. Từ kết quả này hãy đưa ra một số lí do giải thích cho việc vì sao các đồ vật bằng nhôm được sử dụng rất phổ biến.
Lời giải:
= (Al2O3(s)) + 3. (H2(g)) - 2. (Al(s)) - 3. (H2O(l))
= 50,9 + 3.130,7 – 2.28,3 – 3.70,0 = 176,4 J K-1
Ở điều kiện chuẩn T = 298 K
Ta có: = - 298. = -818,3.103 – 298.176,4 = -870867,2 J < 0
rất âm ở điều kiện chuẩn vì thế phản ứng này tự xảy ra.
Các đồ vật bằng nhôm được sử dụng rất phổ biến vì Al phản ứng dễ dàng với H2O ở điều kiện chuẩn để tạo thành lớp màng nhôm oxide Al2O3 bền vững. Lớp màng này bảo vệ cho nhôm kim loại chống lại các tác động ăn mòn của môi trường
Bài tập 3 trang 32 Chuyên đề học tập hóa học 10: Hãy xác định nhiệt độ sôi của CHCl3(l) ở 1 bar và so sánh với giá trị đo được từ thực nghiệm (61,2oC). Giả thiết biến thiên enthalpy và entropy của quá trình không thay đổi theo nhiệt độ.
Biết rằng:
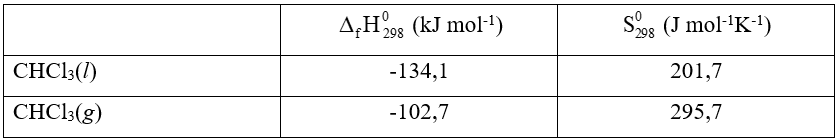
Lời giải:
CHCl3(l) → CHCl3(g)
= ( CHCl3(g)) - (CHCl3(l))
= -102,7 – (-134,1) = 31,4 kJ
∆ = (CHCl3(g)) - (CHCl3(l))
∆ = 295,7 - 201,7 = 94 J K-1
Ở điều kiện chuẩn T = 298 K, 1 bar
Ta có: = - 298. = 31,4.103 – 298.94 = 3388 J
Thực nghiệm T = 61,2 + 273 = 334,2 K
= - 334,2. = 31,4.103 – 334,2.94 = -14,8 J
Thực nghiệm đo được giá trị âm hơn giá trị .
Lời giải bài tập Chuyên đề học tập Hóa học 10 Bài 4: Entropy và biến thiên năng lượng tự do Gibbs Cánh diều hay khác:

