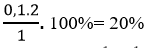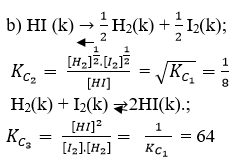Khi đun nóng HI trong một bình kín, xảy ra phản ứng sau 2HI(k) ⇌ H2(k) + I2(k)
Hóa lớp 10 Bài 51: Luyện tập. Tốc độ phản ứng và cân bằng hóa học
Bài 5 (trang 216 sgk Hóa 10 nâng cao): Khi đun nóng HI trong một bình kín, xảy ra phản ứng sau:
2HI(k) ⇌ H2(k) + I2(k)
a) Ở một nhiệt độ nào đó, hằng số cân bằng KC của phản ứng bằng 1/64. Tính xem có bao nhiêu phần trăm HI bị phân hủy ở nhiệt độ đó.
b) Tính hằng số cân bằng KC của hai phản ứng sau ở cùng nhiệt độ như trên:
HI(k) ⇆ 1/2 H2(k) + 1/2 I2(k) và H2(k) + I2(k) ⇆ 2HI(k)
Lời giải:
Gọi KC1,KC2,KC3 lần lượt là các hằng số cân bằng của các phản ứng đã cho.
a)Ta có:
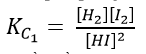
Giả sử ban đầu nồng độ HI là 1 mol/l
Tại thời điểm cân bằng nồng độ HI phân hủy là 2x: [H2] = [I2] = x.
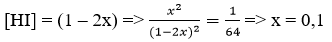
Phần trăm HI bị phân hủy :