Có 100ml H2SO4 98%, khối lượng riêng là l,84g/ml Người ta muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20%
Hóa lớp 10 Bài 45: Hợp chất có oxi của lưu huỳnh
Bài 9 (trang 187 sgk Hóa 10 nâng cao): Có 100ml H2SO4 98%, khối lượng riêng là l,84g/ml. Người ta muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20%.
a) Tính thể tích nước cần dùng để pha loãng.
b) Cách pha loãng phải tiến hành như thế nào?
Lời giải:
a) Ta có:
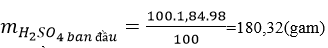
Gọi lượng nước cần pha là m gam
Theo đề bài, ta có: 180,32/(1,84.100 + m) = 20%
Giải ra ta được: m = 717,6 gam vì
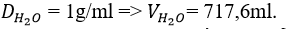
b) Cách pha loãng phải tiến hành như thế nào?
Dùng ống đong, đong 717,6 ml nước đổ vào cốc 1 lít. Sau đó rót từ từ 100ml H2SO4 98% vào cốc đã chứa nước và khuấy đều ta thu được dung dịch H2SO4 20%

