Oleum là gì Hãy xác định công thức của oleum A
Hóa lớp 10 Bài 46: Luyện tập chương 6
Bài 9 (trang 191 sgk Hóa 10 nâng cao): Oleum là gì?
a) Hãy xác định công thức của oleum A, biết rằng sau khi hòa tan 3,38 gam A vào nước, người ta phải cùng 800ml dung dịch KOH 0,1M để trung hòa dung dịch A.
b) Cần hòa tan bao nhiêu gam oleum A vào 200 gam nước để được dung dịch H2SO4 10%?
Lời giải:
Oleum là dung dịch H2SO4 98% hấp thụ SO3 được oleum H2SO4.nSO3 v
H2SO4+ nSO3 → H2SO4.nSO3
a) Xác định công thức oleum.
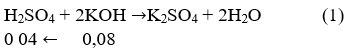
Ta có: nKOH= 0,8.0,1 = 0,08 (mol)
Khi hòa tan oleum vào nước có quá trình:
H2SO4. nSO3 + nH2O → (n + 1) H2SO4 (2)
Từ (2) và đề bài, ta có:
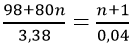
Giải ra được n = 3. Vậy công thức phân tử oleum là: H2SO4. 3SO3.
b) Gọi a là số mol oleum H2SO4. 3SO3
Moleum = 98 + 240 = 338 u => moleum = 338a
Khi hòa tan oleum vào nước có phản ứng sau:
H2SO4.3SO3 + 3H2O → 4H2SO4
1 4
a 4a
Khối lượng H2SO4 khi hòa tan a mol oleum: 98.4a = 392a
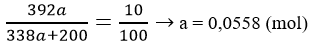
Vậy moleum phải dùng = 338.0,0558 = 18,86 (gam)

