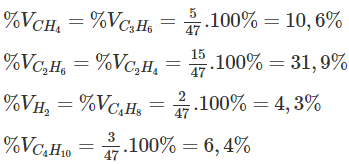Khi crăckinh butan, đã xảy ra các phản ứng: C4H10 -> CH4 + C3H6
Bài 37: Nguồn hiđrocacbon thiên nhiên
Giải bài 6 trang 58 SBT Hóa 11 Bài 37: Nguồn hiđrocacbon thiên nhiên giúp học sinh biết cách làm bài tập trong SBT Hóa 11.
Bài 37.6 trang 58 Sách bài tập Hóa học 11: Khi crăckinh butan, đã xảy ra các phản ứng:
C4H10 → CH4 + C3H6
C4H10 → C2H6 + C2H4
C4H10 → H2 + C4H8
Một phần butan không tham gia các phản ứng.
Hỗn hợp khí A thu được sau phản ứng có thể tích là 47 lít; Dẫn hỗn hợp khí này đi qua nước brom có dư thì thể tích hỗn hợp khí còn lại là 25 lít. Đốt cháy hoàn toàn 5 lít hỗn hợp khí còn lại này thì thu được 9,4 lít CO2. Các thể tích khí đo ở cùng điều kiện.
1. Tính phần trăm thể tích butan đã tham gia các phản ứng.
2. Tính phần trăm theo thể tích của từng khí trong hỗn hợp A nếu biết thêm rằng thể tích C2H4 gấp 3 lần thể tích C3H6.
Lời giải:
C4H10 → CH4 + C3H6
x lít x lít x lít
C4H10 → C2H6 + C2H4
y lít y lít y lít
C4H10 → H2 + C4H8
z lít z lít z lít
Đặt thể tích C4H10 không tham gia phản ứng là t lít.
2x + 2y + 2z + t = 47 (1)
Khi đi qua nước brom dư thì C3H6, C2H4 và C4H8 bị hấp thụ; thể tích các khí còn lại:
x + y + z + t = 25 (2)
Lấy (1) - (2) ta có x + y + z = 22 ; đó chính là thể tích C4H10 đã phản ứng, còn x + y + z + t = 25 cũng chính là thể tích C4H10 trước phản ứng.
Phần trăm theo thể tích của C4H10 phản ứng:
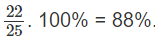
2. Giả sử đốt 25 lít khí còn lại sau khi qua nước brom
CH4 + 2O2 → CO2 + 2H2O
x lít x lít
2C2H6 + 7O2 → 4CO2 + 6H2O
y lít 2y lít
2H2 + O2 → 2H2O
2C4H10 + 13O2 → 8CO2 + 10H2O
t lít 4t lít
Thể tích CO2 thu được sẽ là :
x + 2y + 4t = 47 (3)
Ngoài ra theo đầu bài y = 3x (4)
Giải hệ (1), (2), (3), (4) ta được x = 5; y =15; z = 2; t = 3.
Thành phần phần trăm về thể tích của hỗn hợp A: