Rót dung dịch chứa 11,76 g H3PO4 vào dung dịch chứa 16,8 g KOH. Sau phản ứng cho dung dịch
Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng
Giải bài 9 trang 21 SBT Hóa 11 Bài 13: Luyện tập: Tính chất của nitơ, photpho và các hợp chất của chúng giúp học sinh biết cách làm bài tập trong SBT Hóa 11.
Bài 13.9 trang 21 Sách bài tập Hóa học 11: Rót dung dịch chứa 11,76 g H3PO4 vào dung dịch chứa 16,8 g KOH. Sau phản ứng cho dung dịch bay hơi đến khô. Tính khối lượng muối khan thu được.
Lời giải:
Số mol H3PO4:
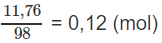
Số mol KOH:
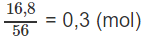
Các phản ứng có thể xảy ra :
H3PO4 + KOH → KH2PO4 + H2O (1)
H3PO4 + 2KOH → K2HPO4 + 2H2O (2)
H3PO4 + 3KOH → K3PO4 + 3H2O (3)
Vì tỉ lệ nKOH : nH3PO4 = 0,3 : 0,12 = 2,5 nằm giữa 2 và 3, nên chỉ xảy ra các phản ứng (2) và (3), nghĩa là tạo ra hai muối K2HPO4 và K3PO4.
Gọi x là số mol H3PO4 tham gia phản ứng (2) và y là số mol H3PO4 tham gia phản ứng (3) :
x + y = 0,12 (a)
Theo các phản ứng (2) và (3) tổng số mol KOH tham gia phản ứng :
2x + 3y = 0,3 (b)
Giải hộ phương trình (a) và (b): x = 0,06 mol K2HPO4 ; y = 0,06 mol K3PO4.
Tổng khối lượng hai muối:
mK2HPO4 + mK3PO4 = 0,06 x 174 + 0,06 x 212 = 10,44 + 12,72 = 23,16 (g).

