Cho 10,6 g hỗn hợp A gồm một kim loại kiềm X và một kim loại kiềm thổ Y
SBT Hóa học 12 Bài 28: Luyện tập: Tính chất của kim loại kiềm, kim loại kiềm thổ và hợp chất của chúng
Giải bài 16 trang 68 SBT Hóa học 12 chi tiết trong bài học Bài 28: Luyện tập: Tính chất của kim loại kiềm, kim loại kiềm thổ và hợp chất của chúng giúp học sinh biết cách làm bài tập Hóa 12.
Bài 28.16 trang 68 Sách bài tập Hóa học 12: Cho 10,6 g hỗn hợp A gồm một kim loại kiềm X và một kim loại kiềm thổ Y tác dụng hết với 300 ml dung dịch HCl 1M (loãng), thu được dung dịch B và 5,6 lít khí (đktc).Dẫn từ từ khí CO2 vào dung dịch B. Số gam kết tủa cực đại thu được là bao nhiêu.
Lời giải:
Đặt hai kim loại là R_ có hoá trị n (1 < n < 2), ta có phương trình cho nhận e:
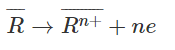
2H+ + 2e → H2
Với số mol H2 là 0,25 (mol) ⟹ số mol R là 0,5/n mol
=> MR = 21,2n
Với 1 ≤ n ≤ 2 → 21,2 ≤ MR ≤ 42,2
Vậy 2 kim loại cần tìm có thể là 2 trong 4 kim loại sau: Na, K, Mg, Ca.
Mặt khác ta có: nHCl = 0,3 mol ⟹ nH2 = 0,15mol, vậy 0,1 mol H2 còn lại do H2O phản ứng tạo ra ⟹ loại Mg vì Mg không phản ứng với nước
⟹ hai kim loại là Na và Ca với số mol tương ứng là x và y
Ta có hệ:
23x + 40y = 10,6 (1)
x + 2y = 0,25.2 = 0,5 (2)
từ (1) và (2) ⟶ x = 0,2 ; y = 0,15
Ta lại có số mol Họ do nước tạo ra là 0,1 mol ⟹ số mol OH- là 0,2 mol
Để tạo kết tủa cực đại tức là toàn bộ CO2 tạo muối CO32-
nOH/nCO2 = 2 => nCO32- = nCO2 = 0,2/2 = 0,1 mol
Vậy kết tủa là CaCO3: 0,1 mol ⟹ m = 0,1.100 = 10 (gam).

