Bài 18.1, 18.2, 18.3, 18.4, 18.5 trang 26 SBT Hóa học 8
Bài 18.1, 18.2, 18.3, 18.4, 18.5 trang 26 SBT Hóa học 8
Bài 18.1 trang 26 sách bài tập Hóa 8: Hãy cho biết số nguyên tử hoặc phân tử có trong lượng chất sau:
- 0,1 mol nguyên tử H - 0,15 mol phân tử CO2;
- 10 mol phân tử H2O; - 0,01 mol phân tử H2;
- 0,24 mol phân tử Fe; - 1,44 mol nguyên tử C;
Lời giải:
- 0,1 mol nguyên tử H = 0,1.6.1023 = 0,6.1023 hoặc 0,1N nguyên tử H.
- 0,15 mol phân tử CO2 = 0,15. 6.1023=0,9. 1023 hoặc 0,15N phân tử CO2.
- 10 mol phân tử H2O = 10. 6.1023 = 60. 1023 hoặc 10N phân tử H2O.
- 0,01 mol phân tử H2 = 0,01. 6.1023 = 0,06. 1023 hoặc 0,01N phân tử H2.
- 0,24 mol nguyên tử Fe = 0,24. 6.1023 = 1,44.1023 hoặc 0,24N nguyên tử Fe.
- 1,44 mol nguyên tử C = 1,44. 6.1023 = 8,64.1023 hoặc 1,44N nguyên tử C
Bài 18.2 trang 26 sách bài tập Hóa 8: Hãy tìm số mol nguyên tử hoặc số mol phân tử của những lượng chất sau:
a) 0,6N nguyên tử O; 1,8N nguyên tử N2; 0,9N nguyên tử H;
1,5N phân tử H2; 0,15N phân tử O2; 0,05N nguyên tử C;
b) 24.1023 phân tử H2O; 1,44.1023 phân tử CO2
0,66.1023 phân tử C12H22O11 (đường)
Lời giải:
a) 0,6N nguyên tử O = 0,6 mol nguyên tử O.
1,8N phân tử N2 = 1,8 mol phân tử N2.
0,9N nguyên tử H = 0,9 mol nguyên tử H.
1,5N phân tử H2 = 1,5 mol phân tử H2.
0,15N phân tử O2 = 0,15 mol phân tử O2.
0,05N nguyên tử C = 0,05 mol nguyên tử C.
b) 24.1023 phân tử H2O =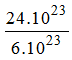
1,44.1023 phân tử CO2 =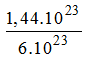
0,66.1023 phân tử C12H22O11 =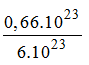
Bài 18.3 trang 26 sách bài tập Hóa 8: Hãy xác định khối lượng của những lượng chất sau đây:
a) 0,01 mol phân tử O; 0,01 mol nguyên tử O2; 2 mol nguyên tử Cu.
b) 2,25 mol phân tử H2O; 0,15 mol phân tử CO2.
c) 0,05 mol của những chất sau: NaCl, H2O, C12H22O11.
Lời giải:
a) mO = nO.MO = 0,01.16 = 0,16(g)
mO2 = nO2.MO = 0,01.32 = 0,32(g)
mCu = nCu.MCu = 2.64 = 128(g)
b) MH2O = 1.2 + 16 = 18 g/mol
mH2O = nH2O.MH2O = 2,25.18 = 40,5(g)
MCO2 = 12 + 16.2 =44g/mol
mCO2 = nCO2.MCO2 = 0,15.44 = 6,6(g)
c) MNaCl = 23 + 35,5 = 58,5 g/mol
mNaCl = nNaCl.MNaCl = 0,05.58,5 = 2,925(g)
mH2O = nH2O.MH2O = 0,05.18 = 0,9(g)
MC12H22O11 = 12.12 + 22 + 16.11 = 324 g/mol
mC12H22O11 = nC12H22O11.MC12H22O11 = 0,05.324 = 17,1(g)
Bài 18.4 trang 26 sách bài tập Hóa 8: Hãy tìm thể tích của những lượng khí sau ở đktc:
a) 0,05 mol phân tử O2; 0,15 mol phân tử H2; 14 mol phân tử CO2.
b) Hỗn hợp khí gồm có: 0,75 mol CO2; 0,25 mol N2; và 0,5 mol O2.
c) 0,02 mol của mỗi chất khí sau: CO, CO2, H2, O2.
Lời giải:
a) VO2 = nO2.22,4 = 0,05.22,4 = 1,12(l)
VH2 = nH2.22,4 = 0,15.22,4 = 3,36(l)
VCO2 = nCO2.22,4 = 14.22,4 = 313,6(l)
b) Vhh = 22,4(nO2 + nH2 + nO2) = 22,4(0,75 + 0,25 + 0,5) = 33,6(l)
c) Ở điều kiện tiêu chuẩn 0,02 mol của các chất khí đều có thể tích bằng nhau:
VCO = VCO2 = VH2 = VO2 = 0,02 . 22,4 = 0,448(l)
Bài 18.5 trang 26 sách bài tập Hóa 8: Hãy xác định khối lượng và thể tích khí ( đktc) của những lượng chất sau:
a) 0,25 mol của mỗi chất khí sau: CH4 (metan), O2, H2, CO2.
b) 12 mol phân tử H2; 0,05 mol phân tử CO2; 0,01 mol phân tử CO.
c) Hỗn hợp khí gồm có: 0,3 mol CO2 và 0,15 mol O2.
Lời giải:
a) MCH4 = 12 + 4 = 16 g/mol
mCH4 = nCH4.MCH4 = 0,25.16 = 4(g)
mO2 = nO2.MO2 = 0,25.32 = 8(g)
mH2 = nH2.MH2 = 0,25. 2 = 0,5(g)
MCO2 = 12 + 16.2 = 44 g/mol
mCO2 = nCO2.MCO2 = 0,25.44 = 11(g)
Ở đktc 0,25 mol của các chất khí đều có thể tích bằng nhau:
VCH4 = VO2 = VH2 = VCO2 = 22,4.0,25 = 5,6(l)
b) mH2 = nH2 .MH2 = 12.2 = 24(g)
→ VH2 = nH2 .22,4 = 12.22,4 = 268,8(l)
mCO2 = nCO2 .MCO2 = 0,05.44 = 2,2(g)
→ VCO2 = nCO2 . 22,4 = 0,05.22,4 = 1,12(l)
mCO = nCO .MCO = 0,01.28 = 0,28(g)
→ VCO = nCO .22,4 = 0,01.22,4 = 0,224(l)
c) mhh = mCO2 + mO2 = (0,3.44) + (0,15.32) = 18(g)
→ VCO = 22,4.(nCO2 + nO2) = 10,08(l)

