Bài 23.3, 23.4, 23.5, 23.6, 23.7, 23.8 trang 31 SBT Hóa học 8
Bài 23.3, 23.4, 23.5, 23.6, 23.7, 23.8 trang 31 SBT Hóa học 8
Bài 23.3 trang 31 sách bài tập Hóa 8: Nung hợp chất canxi cacbonat trong một chén nung, người ta thu được vôi sống có công thức hóa học là CaO và khí thoát ra là CO2. Kết quả của thí nghiệm được ghi lại như sau:
- Khối lượng của chén nung rỗng là 30g.
- Khối lượng của chén nung và canxi cacbonat là 40g.
- Khối lượng của chén nung và CaO là 35,6g.
Hãy điền vào dấu chấm trong những câu sau:
+ Khối lượng của CaO có trong chén sau khi nung là ….g.
+ Số mol của CaO là …
+ Khối lượng khí CO2 thoát ra sau phản ứng là ….g.
+ Số mol của CO2 là …..
+ Phân tử canxi cacbonat bị phân tử thành CaO và CO2, có tỉ lệ số phân tử CaO/ số phân tử CO2 là …/…
Lời giải:
- Khối lượng của CaO có trong chén sau khi nung là: 36,6 – 30 = 5,6(g)
- Số mol:
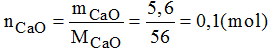
- Khối lượng khí CO2 thoát ra sau phản ứng: 40 – 35,6 = 4,4(g)
- Số mol của khí CO2:
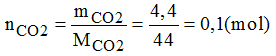
- Phân tử canxi cacbonat bị phân hủy thành CaO và CO2, có tỉ lệ số phân tử CaO:số phân tử CO2 là 1:1.
Bài 23.4 trang 31 sách bài tập Hóa 8: Đốt cháy hoàn toàn cacbon bằng một lượng khí oxi dư, người ta thu được hỗn hợp khí gồm có khí cacbonic (CO2) và khí oxi (O2) dư.
Hãy xác định phần trăm theo khối lượng và thành phần phần trăm theo thể tích của khí oxi trong mỗi hỗn hợp sau:
a) 4g khí cacbonic và 16g khí oxi.
b) 3 mol khí cacbonic và 5 mol khí oxi.
c) 0,3.1023 phân tử CO2 và 0,9.1023 phân tử O2.
Lời giải:



Bài 23.5 trang 31 sách bài tập Hóa 8: Hãy xác định khối lượng và thể tích của những hỗn hợp khí sau ở đktc:
a) 1,5N phân tử oxi + 2,5N phân tử hidro + 0,02N phân tử nito.
b) 1,5 mol phân tử oxi + 1,2 mol phân tử CO2 + 3 mol phân tử nito.
c) 6g hidro + 2,2g khí cacbonic + 1,6g khí oxi.
Lời giải:
a) mO2 = nO2 . MO2 = 1,5 .32 = 48 g
mN2 = nN2 . MN2 = 0,02 . 28 = 0,56 g
mH2 = nH2 . MH2 = 2,5 .2 = 5g
Khối lượng hỗn hợp khí:
mhh = mO2 + mH2 + mN2 = 48 + 5 + 0,56 = 53,56(g)
Thể tích của hỗn hợp khí:
Vhh = 22,4.n = 22,4.( 1,5 + 2,5 + 0,02) = 90,048(l)
b) Tương tự
mO2 = nO2 . MO2 = 1,5 . 32 = 48g
mCO2 = nCO2 . MCO2 = 1,2 . 44 = 52,8 g
mN2 = nN2 . MN2 = 3. 28 = 84g
Khối lượng hỗn hợp khí:
mhh = mO2 + mCO2 + mN2 = 48 + 52,8 + 84 = 184,8 g
Thể tích của hỗn hợp khí:
Vhh = 22,4.n = 22,4.(1,5 + 1,2 + 3) = 127,68 l
Bài 23.6 trang 31 sách bài tập Hóa 8: Đốt cháy hoàn toàn 2,24g Fe, thu được 3,2g oxit sắt. Xác định công thức phân tử của oxit sắt.
Lời giải:
Cách 1: PTHH tổng quát có dạng:

Vậy x = 2; y = 3.
Công thức hóa học của phân tử oxit sắt là Fe2O3.
Cách 2: Khối lượng Oxi trong oxit là: 3,2 – 2,24 = 0,96 g
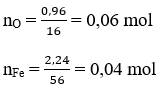
Tỉ lệ nFe : nO = 0,04 : 0,06 = 2:3
⇒ Trong 1 phân tử oxit có 2 nguyên tử Fe, 3 nguyên tử O ⇒ CT oxit là: Fe2O3.
Bài 23.7 trang 31 sách bài tập Hóa 8: Cho dòng khí CO qua hỗn hợp 2 oxit CuO và Fe3O4 nung nóng thu được 29,6g hỗn hợp 2 kim loại trong đó sắt nhiều hơn đồng là 4g.
Tính thể tích khí CO cần dùng (đktc).
Lời giải:
PTHH của các phản ứng:
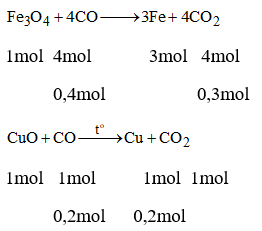
Gọi x là khối lượng của Cu sau phản ứng
→ Khối lượng của sắt sau phản ứng là x+4
Theo đề bài ta có: x + x + 4 = 29,6 → x = 12,8(g)
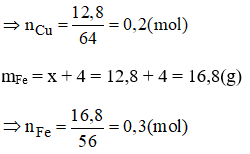
Theo pt:
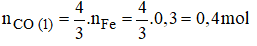
nCO (2) = nCu = 0,2 mol
nCO = (0,4 + 0,2).22,4 = 13,44(l)
Bài 23.8 trang 31 sách bài tập Hóa 8: Cho 20g một oxit sắt phản ứng hết với dung dịch HCl dư, sau phản ứng thu được 40,625g muối clorua. Xác định công thức phân tử của oxit sắt.
Lời giải:
Gọi công thức hóa học của oxit sắt là FexOy
PTHH của phản ứng là:
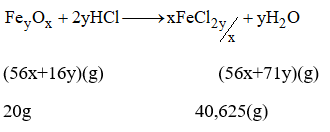
Theo PTHH ta có:
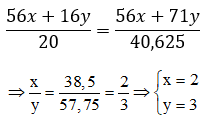
Vậy công thức hóa học của oxit sắt là Fe2O3.

