Bài 42.3, 42.4, 42.5, 42.6, 42.7 trang 58 SBT Hóa học 8
Bài 42.3, 42.4, 42.5, 42.6, 42.7 trang 58 SBT Hóa học 8
Bài 42.3 trang 58 sách bài tập Hóa 8: Để xác định độ tan của một muối trong nước bằng phương pháp thực nghiệm, người ta dựa vào những kết quả sau:
- Nhiệt độ của dung dịch muối bão hòa đo được là 19°C.
- Chén nung rỗng có khối lượng là 47,1g.
- Chén nung đựng dung dịch muối bão hà có khối lượng là 69,6g.
- Chén nung và muối kết tinh thu được sau khi làm bay hết hơi nước, có khôi lượng là 49,6g.
Hãy cho biết:
a) Khối lượng muối kết tinh thu được là bao nhiêu?
b) Độ tan muối ở nhiệt độ 19°C?
c) Nồng độ phần trăm của dung dịch muối bão hòa ở nhiệt độ 19°C?
Lời giải:
a) Khối lượng của muối tinh khiết: 49,6 - 47,1 = 2,5(g)
b) mH2O = 69,6 – 49,6 = 20 (g)
Độ tan của muối ở 19°C
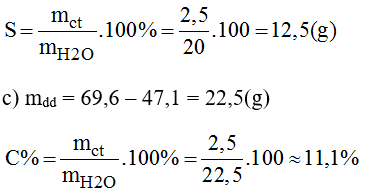
Bài 42.4 trang 58 sách bài tập Hóa 8: Làm bay hơi 300g nước ra khỏi 700g dung dịch muối 12%, nhận thấy 5g muối tách khỏi dung dịch bão hòa. Hãy xác định nồng độ phần trăm của dung dịch muối bão hòa trong điều kiện thí nghiệm trên.
Lời giải:
Khối lượng muối có trog dung dịch ban đầu:
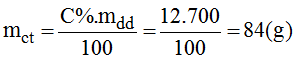
Khối lượng muối có trong dung dịch bão hòa:
mct = mmuối = 84 - 5 = 79(g)
Khối lượng dung dịch muối sau khi bay hơi:
mdd = 700 – (300 + 5) = 395(g)
Nồng độ phần trăm của dung dịch bão hòa:
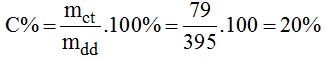
Bài 42.5 trang 58 sách bài tập Hóa 8: Một dung dịch CuSO4 có khối lượng riêng là 1,206g/ml. Khi cô cạn 165,84ml dung dịch này người ta thu được 36g CuSO4. Hãy xác định nồng độ phần trăm của dung dịch CuSO4 đã dùng.
Lời giải:
Khối lượng dung dịch CuSO4 ban đầu:
mdd = V.D = 165,84.1,206 = 200(g)
Nồng độ % của dung dịch CuSO4:
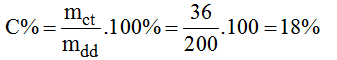
Bài 42.6 trang 58 sách bài tập Hóa 8: Hãy điền vào những ô trống của bảng những số liệu thích hợp của mỗi dung dịch glucozo C6H12O6 trong nước:
| Các dung dịch | Khối lượng C6H12O6 | Số mol C6H12O6 | Thể tích dung dịch | Nồng độ mol CM |
| Dung dịch 1 | 12,6(g) | .... | 219ml | .... |
| Dung dịch 2 | .... | 1,08mol | .... | 0,519M |
| Dung dịch 3 | .... | .... | 1,62l | 1,08M |
Lời giải:
| Các dung dịch | Khối lượng C6H12O6 | Số mol C6H12O6 | Thể tích dung dịch | Nồng độ mol CM |
| Dung dịch 1 | 12,6(g) | 0,07mol | 219ml | 0,32M |
| Dung dịch 2 | 194,4g | 1,08mol | 2081ml | 0,519M |
| Dung dịch 3 | 315g | 1,75mol | 1,62l | 1,08M |

Để tính tương tự dung dịch 2, 3 ta được kết quả trong bảng trên.
Bài 42.7 trang 58 sách bài tập Hóa 8: Trình bày phương pháp thực nghiệm để xác định nồng độ phần trăm và nồng độ ml của mẫu dung dịch CuSO4 có sẵn trong phòng thí nghiệm.
Lời giải:
* Phương pháp xác định nồng độ phần trăm dung dịch CuSO4
- Cân một lượng dung dịch CuSO4 xác định.
- Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng đó là CuSO4. Sau đó đem cân lượng muối sau khi cô cạn này ta được số liệu là mct.
- Áp dụng công thức: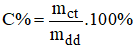
* Phương pháp xác định nồng độ mol của dung dịch CuSO4:
- Đong 1 thể tích dung dịch CuSO4 xác định, đem cân lượng dung dịch đó.
- Sau đó dùng công thức n = m/M để tính số mol của CuSO4.
- Tính nồng độ mol của dung dịch CuSO4 bằng công thức: CM = n/V

