Bài 29.5, 29.6, 29.7, 29.8, 29.9, 29.10, 29.11, 29.12 trang 41 SBT Hóa học 8
Bài 29.5, 29.6, 29.7, 29.8, 29.9, 29.10, 29.11, 29.12 trang 41 SBT Hóa học 8
Bài 29.5 trang 41 sách bài tập Hóa 8: Khi đun nóng kali clorat KClO3 ( có chất xúc tác), chất này bị phân hủy tạo thành kali clorua và khí oxi.
Tính khối lượng kali clorua cần thiết để sinh ra một lượng oxi đủ đốt cháy hết 3,6g cacbon.
Lời giải:
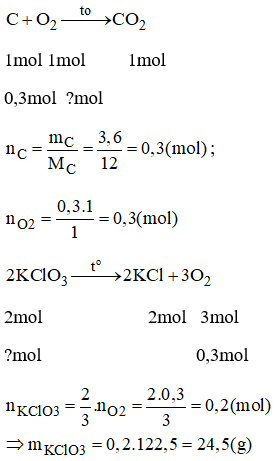
Bài 29.6 trang 41 sách bài tập Hóa 8: Đốt cháy 6,2g photpho trong bình chứa 7,84 lit oxi (đktc). Hãy cho biết sau khi cháy:
a) Photpho hay oxi, chất nào còn thừa và khối lượng là bao nhiêu?
b) Chất nào được tạo thành và khối lượng là bao nhiêu?
Lời giải:
a)
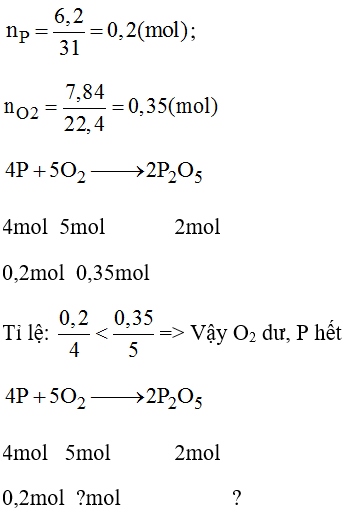
Số mol của oxi tham gia phản ứng:
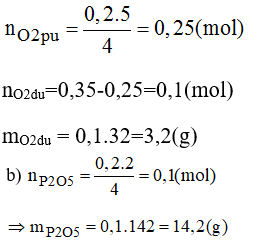
Bài 29.7 trang 41 sách bài tập Hóa 8: Xác định công thức hóa học một oxi của lưu huỳnh có khối lượng mol là 64g và biết thành phần phần trăm về khối lượng của nguyên tố lưu huỳnh trong oxit là 50%.
Lời giải:
Công thức hóa học: SxOy
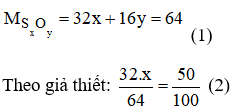
Giải phương trình (2) ta được: x = 1 thay vào pt (1) ⇒ y = 2.
Vậy công thức hóa học của oxit là SO2.
Bài 29.8 trang 41 sách bài tập Hóa 8: Một oxit của photpho có thành phần phần trăm của P bằng 43,66%. Biết phân tử khối của oxit bằng 142 đvC. Công thức hóa học của oxit là:
A. P2O5 B.P2O4 C.PO2 D.P2O4.
Lời giải:
Gọi công thức hóa học của photpho: PxOy
%O = 100 – 43,66 = 5,34%
MPxOy = 31x + 16y = 142
Tỉ lệ khối lượng:
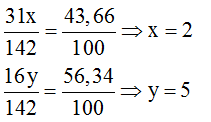
Vậy công thức hóa học của oxit photpho là P2O5.
Chọn B.
Bài 29.9 trang 41 sách bài tập Hóa 8: Trong phòng thí nghiệm khi đốt cháy sắt trong oxi ở nhiệt độ cao được oxit sắt từ (Fe3O4).
a) Số gam sắt và khí oxi cần dùng điều chế 2,32g oxit sắt từ lần lượt là:
A. 0,84g và 0,32g B. 2,52g và 0,96g
C. 1,86g và 0,64g D. 0,95g và 0,74g
Hãy giải thích sự lựa chọn.
b) Số gam kali pemanganat KMnO4 cần dùng để điều chế lượng khí oxi cần dùng cho phản ứng trên là:
A.3,16g B. 9,48g C.5,24g D.6,32g
Hãy giải thích sự lựa chọn.
Lời giải:
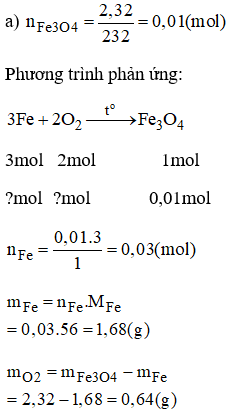
→ Đáp án C.
b) Theo câu a: số mol của O2: nO2 = 0,02mol
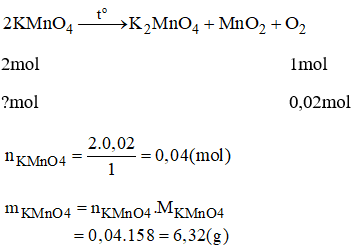
Bài 29.10 trang 41 sách bài tập Hóa 8: Một oxit được tạo bởi 2 nguyên tố sắt và oxi trong đó tỉ lệ khối lượng giữa sắt và oxi là 7/3. Tìm công thức phân tử của oxit đó.
Lời giải:
Gọi công thức hóa học của oxit sắt là: FexOy:
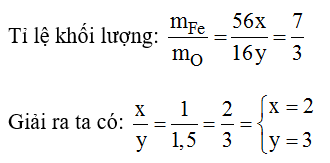
Công thức hóa học: Fe2O3.
Bài 29.11 trang 41 sách bài tập Hóa 8: Tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau:
a) Khi đốt 0,3 mol cacbon trong bình chứa 4,48lit khí oxi ( đktc)
b) Khi đốt 6g cacbon trong bình chứa 13,44 lit khí oxi.
Lời giải:
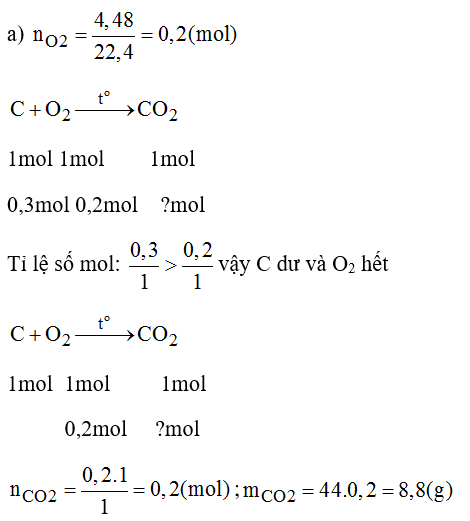
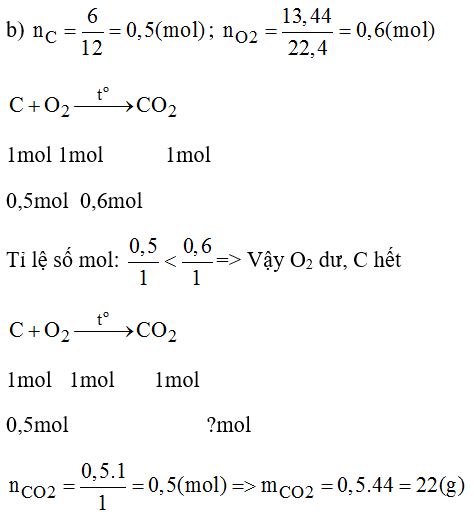
Bài 29.12 trang 41 sách bài tập Hóa 8: Nung a g KClO3 và b g KMnO4 thu được cùng một lượng O2. Tính tỉ lệ a/b.
Lời giải: