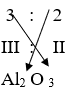Giáo án KHTN 7 Bài 7: Hóa trị và công thức hóa học - Kết nối tri thức
Giáo án KHTN 7 Bài 7: Hóa trị và công thức hóa học - Kết nối tri thức
Chỉ 400k mua trọn bộ Giáo án KHTN 7 Kết nối tri thức bản word chuẩn kiến thức, trình bày đẹp mắt:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
Thời gian thực hiện: 3 tiết
I. MỤC TIÊU
1. Kiến thức
- Trình bày được khái niệm về hóa trị(cho chất cộng hóa trị), cách viết công thức hóa học.
- Viết được công thức hóa học của một số đơn chất và hợp chất đơn giản, thông dụng.
- Nêu được mối liên hệ giữa hóa trị của nguyên tố với công thức hóa học của hợp chất.
- Tính được phần trăm nguyên tố trong hợp chất khi biết công thức hóa học của nó.
- Xác định công thức hóa học của hợp chất dựa vào phần trăm nguyên tố và khối lượng phân tử.
2. Năng lực
2.1. Năng lực chung
- Năng lực tự chủ và tự học:Tìm kiếm thông tin, đọc sách giáo khoa, quan sát hình, để tìm hiểu về hóa trị, quy tắc hóa trị, cách lập công thức hóa học, cách tính phần trăm của nguyên tố trong hợp chất.
- Năng lực giao tiếp và hợp tác:Thảo luận nhóm để trả lời câu hỏi.
- Năng lực giải quyết vấn đề và sáng tạo:Giải quyết vấn đề trong xác định phần trăm nguyên tố trên các bao bì, nhãn mác, chai lọ trên đồ ăn, đồ uống, bánh kẹo, phân bón...
2.2. Năng lực khoa học tự nhiên
- Năng lực nhận biết KHTN:Nhận biết hóa trị của nguyên tố và nhóm nguyên tử.
- Năng lực tìm hiểu tự nhiên:Viết đúng công thức hóa học của các đơn chất, hợp chất, tính phần trăm của nguyên tố khi biết công thức hóa học của hợp chất, lập công thức hóa học khi biết phần trăm nguyên tố và khối lượng phân tử của hợp chất đó.
- Vận dụng kiến thức, kỹ năng đã học: Tính được phần trăm của các nguyên tố trong hợp chất trên các bao bì, nhãn mác đồ ăn, đồ uống, phân bón...trong thực tế.
3. Phẩm chất
- Chăm học, chịu khó tìm tòi tài liệu và thực hiện các nhiệm vụ cá nhân nhằm tìm hiểu về hóa trị, lập công thức hóa học, tính phần trăm nguyên tố trong hợp chất.
- Có trách nhiệm trong hoạt động nhóm, chủ động nhận và thực hiện nhiệm vụ tìm hiểu về quy tắc hóa trị.
-Trung thực, cẩn thận trong xác định thành phần nguyên tố các chất trên bao bì, nhãn mác các hợp chất trong thực tế.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Giáo viên
- Thiết kế các phiếu học tập.
- Thông tin về phần trăm khối lượng nguyên tố trên một số bao bì đồ ăn, nước uống, phân bón….
- Hình ảnh về vật dụng trong đời sống như: dây đồng, con dao, cái kéo, các chất trong đời sống như nước, muối ăn….
2. Học sinh
-Ôn tập bài cũ và chuẩn bị bài mới.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG MỞ ĐẦU
a) Mục tiêu: Xác định vấn đề học tập là xác định mối liên hệ giữa hóa trị và công thức hóa học của chất.
b) Nội dung:
- Học sinh thực hiện nhiệm vụ cá nhân quan sát mô hình phân tử nước, hoạt động cá nhân trả lời câu hỏi.
c)Sản phẩm:
- Học sinh nêu được: Các nguyên tố hóa học liên kết với nhau theo hóa trị tạo thành hợp chất.
d)Tổ chức thực hiện:
Hoạt động của giáo viên và học sinh |
Nội dung |
|
*Chuyển giao nhiệm vụ học tập - GV: chiếu hình ảnh mô hình phân tử nước, yêu cầu HS hoạt động cá nhân đọc thông tin, quan sát mô hình và trả lời câu hỏi: ? Hóa trị có mối liên hệ với công thức hóa học của hợp chất như thế nào? - HS nhận nhiệm vụ. * Thực hiện nhiệm vụ học tập - HS hoạt động cá nhân theo yêu cầu của GV trả lời câu hỏi. - GV theo dõi và hỗ trợ HS. * Báo cáo kết quả và thảo luận - GV gọi ngẫu nhiên học sinh trình bày đáp án. - HS trình bày. * Đánh giá kết quả thực hiện nhiệm vụ - Học sinh nhận xét, bổ sung, đánh giá. - Giáo viên nhận xét, đánh giá. Þ Giáo viên gieo vấn đề cần tìm hiểu trong bài học: Để trả lời câu hỏi trên đầy đủ và chính xác nhất chúng ta vào bài học hôm nay. |
Dự kiến sản phẩm HS trả lời:Các nguyên tố hóa học liên kết với nhau theo hóa trị tạo thành hợp chất. |
B. HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Tìm hiểu về công thức hóa học
a) Mục tiêu
- Biết cách viết công thức hóa học của hợp chất, đơn chất.
- Tính được phần trăm nguyên tố trong hợp chất khi biết công thức hóa học.
b) Nội dung
- Học sinh làm việc theo cặp đôi (cùng bàn) nghiên cứu thông tin trong SGK hoàn thiện bảng – phiếu học tập số 1; HS hoạt động cá nhân trả lời các câu hỏi vấn đáp của GV từ đó hình thành kiến thức.
PHIẾU HỌC TẬP SỐ 1
Các hợp chất thông dụng |
Nguyên tố hóa học tạo nên hợp chất |
Số nguyên tử của mỗi nguyên tố |
Khối lượng phân tử |
Ammonia, NH3 |
|||
Saccarose (Đường ăn), C12H22O11 |
|||
Sodium chloride (Muối ăn), NaCl |
|||
Nước, H2O |
|||
Sodium bicarbonate, NaHCO3 |
c) Sản phẩm:
- Câu trả lời của HS.
TRẢ LỜI PHIẾU HỌC TẬP SỐ 1
Các hợp chất thông dụng |
Nguyên tố hóa học tạo nên hợp chất |
Số nguyên tử của mỗi nguyên tố |
Khối lượng phân tử |
Ammonia, NH3 |
N, H |
1 N, 3 H |
17 amu |
Saccarose (Đường ăn), C12H22O11 |
C, H, O |
12 C, 22 H, 11 O |
342 amu |
Sodium chloride (Muối ăn), NaCl |
Na, Cl |
1 Na, 1 Cl |
58,5 amu |
Nước, H2O |
H, O |
2 H, 1 O |
18 amu |
Sodium bicarbonate, NaHCO3 |
Na, H, C, O |
1 Na, 1 H, 1 C, 3 O |
84 amu |
d) Tổ chức thực hiện:
|
Hoạt động của giáo viên và học sinh |
Nội dung |
|
* Chuyển giao nhiệm vụ học tập. - Yêu cầu HS đọc thông tin SGk trả lời câu hỏi. ? Công thức hóa học của một chất được biểu diễn như thế nào? ? Công thức hóa học của đơn chất được biểu diễn như thế nào? Nêu ví dụ? (Hoặc có thể hỏi những đơn chất nào có KHHH được coi là CTHH của chính nó? Lấy ví dụ?) ? Công thức hóa học của hợp chất được biểu diễn như thế nào? Nêu ví dụ? Em có hiểu biết gì về chỉ số chân có ở trong CTHH của hợp chất? ? Nêu ý nghĩa của công thức hóa học? - Yêu cầu HS hoạt động nhóm hoàn thành phiều học tập số 1. * Thực hiện nhiệm vụ học tập. - Học sinh hoạt động cặp đôi trả lời câu hỏi, HS hoạt động cặp đôi hoàn thành phiếu học tập. - GV quan sát tổng quát. * Báo cáo kết quả và thảo luận. GV môt sô HS trình bày, các HS khác bổ sung. * Đánh giá kết quả thực hiện nhiệm vụ. - Học sinh nhận xét, bổ sung, đánh giá. - Giáo viên nhận xét, đánh giá. - GV nhận xét và chốt nội dung về cách viết công thức hóa học của đơn chất, hợp chất, ý nghĩa - Yêu cầu HS hoạt động cá nhân tìm hiểu số nguyên tử của từng nguyên tố trong hợp chất và cách tính phần trăm khối lượng các nguyên tố trong hợp chất copper sulfate (CuSO4). |
I.Công thức hóa học - CTHH của một chất là cách biểu diễn chất bằng kí hiệu hóa học của nguyên tố kèm theo chỉ số ở chân bên phải nguyên tố. - Đối với các đơn chất tạo thành từ nguyên tố kim loại, khí hiếm và một số phi kim (rắn) thì kí hiệu hóa học của nguyên tố coi là công thức hóa học. + Ví dụ: CTHH của sắt là Fe, của đồng là Cu, của carbon là C…. - Một số phi kim có thêm chỉ số chân ở bên phải KHHH. Ví dụ: Khí oxygen có CTHH là O2 … - Công thức hóa học của hợp chất gồm kí hiệu hóa học của nguyên tố và chỉ số chân ở bên phải của kí hiệu hóa học. Ví dụ: Sodium chloride : NaCl - Chỉ số chân là: số nguyên, chỉ số nguyên tử của mỗi nguyên tố có trong hợp chất đang xét, chỉ số bằng 1 thì không ghi. - Ý nghĩa của CTHH: Công thức hoá học cho biết: + Các nguyên tố hóa học tạo nên chất. + Số nguyên tử hay tỉ lệ số nguyên tử của các nguyên tố hóa họccó trong phân tử. + Khối lượng phân tử của chất Lời giải phiếu học tập số 1 (mục sản phẩm). - Số nguyên tử của từng nguyên tố: 1Cu, 1S, 4O.
Hoặc (%O = 100% - 40% - 20% = 40%) |
Hoạt động 2: Tìm hiểu khái niệm hóa trị
a) Mục tiêu
- Nêu khái niệm hóa trị.
- Xác định hóa trị của chlorine trong mô hình.
b) Nội dung
- Học sinh làm việc cá nhân nghiên cứu thông tin trong SGK trả lời câu hỏi.
c) Sản phẩm
- Câu trả lời của học sinh.
d) Tổ chức thực hiện
Hoạt động của giáo viên và học sinh |
Nội dung |
|
*Chuyển giao nhiệm vụ học tập. - Yêu cầu học sinh hoạt động cá nhânđọc thông tin và trả lời câu hỏi: ? Hóa trị là gì? Trong chất cộng hóa trị, hóa trị của nguyên tố được xác định như thế nào? ? Quan sát ?2/42- Mô hình sự hình thành liên kết cộng hóa trị trong phân tử HCl. Hãy xác định hóa trị của chlorine trong mô hình? *Thực hiện nhiệm vụ học tập. - Học sinh hoạt động cá nhân trả lời câu hỏi. - GV quan sát tổng quát. *Báo cáo kết quả và thảo luận. GV gọi ngẫu nhiên một HS trình bày, các HS khác bổ sung. *Đánh giá kết quả thực hiện nhiệm vụ. - Học sinh nhận xét, bổ sung, đánh giá. - Giáo viên nhận xét, đánh giá. - GV nhận xét và chốt nội dung. |
II. Hoá trị 1. Khái niệm hoá trị - Hóa trị là con số biểu thị khả năng liên kết của nguyên tử nguyên tố này với nguyên tử nguyên tố khác. - Trong chất cộng hóa trị, hóa trị của nguyên tố được xác định bằng số cặp electron dùng chung của nguyên tử nguyên tố đó với nguyên tử khác. - Trong phân tử HCl, nguyên tử Cl có 1 cặp eletron dùng chung với nguyên tử H. Do vậy Cl có hóa trị I. |
Hoạt động 3: Tìm hiểu về quy tắc hóa trị
a) Mục tiêu
- Nêu quy tắc hóa trị.
- Xác định hóa trị của nguyên tố trong hợp chất.
- Nắm được hóa trị của các nguyên tố, nhóm nguyên tử trong bảng 7.2, 7.3, viết đúng công thức hóa học của hợp chất dựa vào hóa trị của nguyên tố.
b) Nội dung
- Học sinh làm việc cá nhân nghiên cứu thông tin trong SGK bảng 7.1, thảo luận nhóm trả hoàn thành bảng trả lời câu hỏi.
c) Sản phẩm:
- Các câu trả lời của HS.
d) Tổ chức thực hiện
Hoạt động của giáo viên và học sinh |
Nội dung |
|
*Chuyển giao nhiệm vụ học tập 1. - Yêu cầu học sinh hoạt động cá nhân đọc thông tin bảng 7.1 và trả lời câu hỏi: ? Xét phân tử H2S, hãy so sánh tích của chỉ số và hóa trị của nguyên tố lưu huỳnh với tích của chỉ số và hóa trị của nguyên tố hydrogen? ? Xét phân tử CH4, hãy so sánh tích của chỉ số và hóa trị của nguyên tố carbon với tích của chỉ số và hóa trị của nguyên tố hydrogen? ? Từ kết quả so sánh trên hãy rút ra quy tắc hóa trị với hợp chất 2 nguyên tố. *Thực hiện nhiệm vụ học tập. - Học sinh thảo luận nhóm trả lời trả lời câu hỏi: - GV bao quát tổng quát, theo dõi hoạt động của các nhóm, ghi chép làm căn cứ đánh giá sự tích cực của các nhóm. *Báo cáo kết quả và thảo luận. GV yêu cầu một nhóm báo cáo, các nhóm khác bổ sung. *Đánh giá kết quả thực hiện nhiệm vụ. - Học sinh nhận xét, bổ sung, đánh giá. - Giáo viên nhận xét, đánh giá chuẩn hoá kiến thức. *Chuyển giao nhiệm vụ học tập 2. - GV sử dụng kỹ thuật các mảnh ghép yêu cầu HS hoàn thành ? 1,2,3/43. ? 1: Xác định hóa trị của lưu huỳnh trong hợp chất sulfur dioxide (một nguyên tử S liên kết với 2 nguyên tử O). ? 2: Hãy xác định hóa trị của carbon trong hợp chất methane có trong hình 5.3b. ? 3: Dựa vào quy tắc hóa trị và bảng 7.2, cho biết công thức hóa học của potassium oxide là KO hay K2O *Thực hiện nhiệm vụ học tập. + Vòng chuyên gia: Nhóm 1, 2 hoàn thành câu 1. Nhóm 3, 4 hoàn thành câu 2. Nhóm 5, 6 hoàn thành câu 3. + Vòng mảnh ghép: Các nhóm mảnh ghép thảo luận hoàn thành 3 câu hỏi/ 43 *Báo cáo kết quả và thảo luận. - Các nhóm báo cáo, nhận xét, bổ sung. - Gv nhận xét và chốt lại. *Đánh giá kết quả thực hiện nhiệm vụ. - Học sinh nhận xét, bổ sung, đánh giá. - Giáo viên nhận xét, đánh giá. - GV nhận xét và chuẩn hoá kiến thức. |
2. Quy tắc hoá trị - Xét phân tử H2S Ta thấy: 1.II = 2.I ⇒ Tích của chỉ số và hóa trị của nguyên tố lưu huỳnh bằng tích của chỉ số và hóa trị của nguyên tố hydrogen. - Xét phân tử CH4. Ta thấy: 1.IV = 4.I ⇒ Tích của chỉ số và hóa trị của nguyên tố carbon bằng tích của chỉ số và hóa trị của nguyên tố hydrogen. Nhận xét: Trong công thức hóa học của hợp chất hai nguyên tố tích, chỉ số và hóa trị của nguyên tố này bằng tích chỉ số và hóa trị của nguyên tố kia. ? 1: Oxygen được quy ước có hóa trị II. Hợp chất sulfur dioxide (SO2), nguyên tử nguyên tố S liên kết được với hai nguyên tử O nên có hóa trị IV ? 2: Quy ước nguyên tố H có hóa trị I. Nguyên tử C liên kết được với 4 nguyên tử H nên nguyên tử C có hóa trị IV. ?3: Theo bảng 7.2, nguyên tố K có hóa trị I, nguyên tố O có hóa trị II. Giả sử, công thức hóa học của potassium oxide là KO. Theo quy tắc hóa trị: 1.I ≠ 1.II ⇒ Giả sử sai. ⇒ Công thức hóa học của potassium oxide là K2O Theo quy tắc hóa trị: 2.I = 1.II (thỏa mãn). |
Hoạt động 4: Lập công thức hóa học của hợp chất khi biết hóa trị.
a) Mục tiêu
- Biết lập công thức hóa học của hợp chất khi biết hóa trị.
b) Nội dung
- HS lập được công thức hóa học của hợp chất khi biết hóa trị theo quy tắc chéo.
c)Sản phẩm
- Câu trả lời của học sinh.
d)Tổ chức thực hiện:
Hoạt động của giáo viên và học sinh |
Nội dung |
|
*Chuyển giao nhiệm vụ học tập. - Yêu cầu HS hoạt động cá nhân đọc ví dụ SGK về lập CTHH của lưu huỳnh hóa trị IV và oxygen hóa trị II. *Thực hiện nhiệm vụ học tập. - HS tìm hiểu cách lập CTHH của S(IV) và O(II) - HĐ theo nhóm, mỗi nhóm làm 1 ý: Vận dụng: Lập công thức hóa học của các chất tạo nên bởi: 1. Al(III) và O(II) 2. Fe(III) và Cl(I) 3. K(I) nhóm SO4(II) *Báo cáo kết quả : -Học sinh trả lời, HS khác bổ sung *Đánh giá kết quả thực hiện nhiệm vụ. - Học sinh nhận xét, bổ sung, đánh giá. - GV hướng dẫn HS lập nhanh CTHH theo quy tắc chéo như sau: + Viết kí hiệu hóa học của nguyên tố hay nhóm nguyên tử đứng cạnh nhau. + Viết hóa trị tương ứng lên phía trên. + Rút gọn tỉ lệ hóa trị thành phân số tối giản. + Quy tắc chéo: Hóa trị rút gọn nguyên tố này là chỉ số của nguyên tố kia, hóa trị rút gọn nguyên tố kia là chỉ số nguyên tố này. |
III. Lập công thức hoá học của hợp chất 1. Lập công thức hoá học của hợp chất khi biết hoá trị 1. Đặt công thức của Al(III) và O(II) là Theo quy tắc hóa trị: x.III = y.II ⇒ Lấy x = 2 và y = 3. Vậy công thức cần lập là Al2O3. 2. Đặt công thức của Fe(III) và Cl(I) là Theo quy tắc hóa trị: x.III = y.I ⇒ Lấy x = 1 và y = 3. Vậy công thức cần lập là FeCl3. 3. Đặt công thức của K(I) và SO4(II) là Theo quy tắc hóa trị: x.I = y.II ⇒ Lấy x = 2 và y = 1. Vậy công thức cần lập là K2SO4. |
Hoạt động 5. Lập công thức hóa học của hợp chất theo phần trăm các nguyên tố.
a) Mục tiêu
- Biết lập công thức hóa học của hợp chất khi biết phần trăm các nguyên tố.
b) Nội dung
- HS làm việc cá nhân hoặc nhóm, lập thức hóa học của hợp chất khi biết phần trăm của nguyên tố trong hợp chất.
c)Sản phẩm
- Công thức hóa học đúng của một số hợp chất.
d)Tổ chức thực hiện
Hoạt động của giáo viên và học sinh |
Nội dung |
|
*Chuyển giao nhiệm vụ học tập. - Yêu cầu HS hoạt động cá nhân tìm hiểu cách lập công thức hóa học của hợp chất tạo bởi carbon và hydrogen. Sau đó thảo luận nhóm hoàn thành bài tập trong sách: ?1: Khí carbondioxide luôn có thành phần như sau: Cứ 1 phần khối lượng carbon tương ứng với 2,667 phần khối lượng oxygen. Hãy lập CTHH của khí carbon dioxide, biết khối lượng phân tử của nó là 44 amu. ?2: Hãy lập công thức phân tử của khí hydrogen sulfide, biết lưu huỳnh trong hợp chất này có hóa trị II. Tính phần trăm về khối lượng của lưu huỳnh và hydrogen trong hợp chất đó. *Thực hiện nhiệm vụ học tập - HS làm bài tập. *Báo cáo kết quả - Học sinh trả lời, hs khác bổ sung. *Đánh giá kết quả thực hiện nhiệm vụ - Học sinh nhận xét, GV chuẩn hoá kiến thức. |
2. Lập công thức hoá học của chất theo phần trăm các nguyên tố ?1: Đặt công thức của khí carbon dioxide là CxOy. Khối lượng phân tử của khí carbon dioxide là: 12.x + 16.y = 44 Ta có: ⇒⇒ y = 2x Thay y = 2x vào phương trình khối lượng phân tử được: 12.x + 16.2x = 44 ⇒ x = 1, vậy y = 2. Vậy công thức của khí carbon dioxide là CO2. ?2: Đặt công thức của khí hydrogen sulfide là Theo quy tắc hóa trị: x.I = y.II ⇒ Lấy x = 2 và y = 1. Vậy công thức của khí hydrogen sulfide là H2S. ⇒ Khối lượng phân tử của khí hydrogen sulfide là: 2.1 + 32 = 34 (amu). Phần trăm về khối lượng của lưu huỳnh và của hydrogen trong H2S là:
|
C. HOẠT ĐỘNG LUYỆN TẬP
a) Mục tiêu
- Viết đúng công thức của đơn chất kim loại, phi kim, khí hiếm.
- Lập công thức hóa học của hợp chất khi biết hóa trị của nguyên tố hoặc phần trăm khối lượng nguyên tố và khối lượng phân tử.
b) Nội dung
- HS hoạt động cá nhân, hoạt động nhóm trả lời.
c)Sản phẩm
- Viết đúng công thức hóa học của đơn chất, hợp chất.
d)Tổ chức thực hiện:
Hoạt động của giáo viên và học sinh |
Nội dung |
|
*Chuyển giao nhiệm vụ học tập GV sử dụng kỹ thuật khăn trải bàn yêu cầu HS hoạt động cá nhân trả lời câu hỏi, sau đó thảo luận nhóm thống nhất đáp án thực hiện nhiệm vụ sau: 1. Lập nhanh CTHH của hợp chất tạo bởi: a. Mg hóa trị II và O hóa trị II. b. Fe hóa trị III và O hóa trị II. c. H hóa trị I vànhóm SO4 hóa trị II. 2. Xác định hóa trị của sắt có trong hợp chất Fe2O3 và FeCl2, biết Cl hóa trị I, O hóa trị II. 3. Lập công thức hóa học của khí tạo bởi carbon và oxygen, trong đó carbon chiếm 43% còn lại là oxygen và khối lượng phân tử là 28 amu. *Thực hiện nhiệm vụ học tập - HS hoạt động cá nhân hoàn thành các câu hỏi. - HS thảo luận theo nhóm thống nhất đáp án. *Báo cáo kết quả và thảo luận - Các nhóm báo cáo kết quả, các nhóm khác bổ sung. *Đánh giá kết quả thực hiện nhiệm vụ - HS đánh giá, nhận xét. - GV đánh giá hoạt động cá nhân và hoạt động thảo luận nhóm, chốt lại nội dung kiến thức. |
Luyện tập 1. a. MgO b. Fe2O3 c. H2SO4 2. - Trong công thức Fe2O3: Theo quy tắc hóa trị ta có: (Hóa trị Fe).2 = 3.II Þ Hóa trị Fe = III. - Trong công thức FeCl2: Theo quy tắc hóa trị ta có: (Hóa trị Fe).1 = 2.I Þ Hóa trị Fe = II 3: - Ta có: %O = 100% - 43% = 57% - Đặt công thức của hợp chất là: CxOy. - Khối lượng phân tử: x.12 + y.16 = 28
x = 1
y = 1 Vậy công thức của hợp chất là: CO |
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu
- Viết đúng một số công thức của các chất trong đời sống thường gặp.
- HS hiểu được các số liệu ghi trên bao bì đồ ăn, đồ uống, phân bón....
b) Nội dung
- HS quan sát vật dụng bằng kim loại như dao, kéo, thau, dây điện bằng đồng, viết đúng công thức của các đơn chất có trong các vật dụng trên.
- HS quan sát một số bao bì, tính được phần trăm khối lượng các nguyên tố trên bao bì.
c)Sản phẩm
- Các câu trả lời của học sinh.
d) Tổ chức thực hiện
Hoạt động của giáo viên và học sinh |
Nội dung |
|
*Chuyển giao nhiệm vụ học tập - Yêu cầu HS quan sát hình ảnh về các vật dụng dây đồng, dao, kéo, một số chất như nước, muối ăn, hình ảnh bao bì phân bón NPK. Hãy hoạt động cá nhân trả lời câu hỏi. 1. Viết CHTT của chất tạo nên các vật dụng như dao, kéo, dây đồng. 2. Các chất như muối ăn, nước có công thức hóa học như thế nào? 3. Tính phần trăm khối lượng nguyên tố N trong công thức NH3 và trong NH4NO3. *Thực hiện nhiệm vụ học tập. - HS hoạt động cá nhân thực hiện nhiệm vụ. *Báo cáo kết quả và thảo luận - Đại diện 3 HS trình bày, các HS khác chú ý theo dõi nhận xét. *Đánh giá kết quả thực hiện nhiệm vụ - GV nhận xét và chốt lại đáp án. |
1. - Dao, kéo được tạo thành từ đơn chất sắt có CTHH là Fe. - Dây đồng dùng làm dây dẫn điện có CTHH là Cu. 2. Muối ăn có CTHH là NaCl, nước có CTHH là H2O. 3. Trong công thức NH3
Trong công thức NH4 NO3
|
................................
................................
................................
Trên đây tóm tắt một số nội dung có trong bộ Giáo án Khoa học tự nhiên 7 Kết nối tri thức năm 2023 mới nhất, để mua tài liệu đầy đủ, Thầy/Cô vui lòng: