Cho phương trình nhiệt hóa học sau:2H2 (g) + O2 (g) ⟶ 2H2O (g) delta r H 0 298 = − 483,64 kJSo sánh đúng là
Câu hỏi:
Cho phương trình nhiệt hóa học sau:
2H2 (g) + O2 (g) ⟶ 2H2O (g) 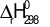 = − 483,64 kJ
= − 483,64 kJ
So sánh đúng là
A. 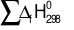 (cđ) >
(cđ) >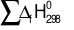 (sp);
(sp);
B. 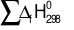 (cđ) =
(cđ) = 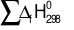 (sp);
(sp);
C. 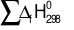 (cđ) <
(cđ) <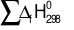 (sp);
(sp);
D. 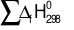 (cđ) ≤
(cđ) ≤ 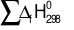 (sp).
(sp).
Trả lời:
Đáp án đúng là: A
Ta có: 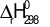 =
= 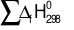 (sp) –
(sp) – 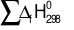 (cđ)
(cđ)
Với 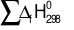 (cđ);
(cđ); 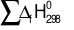 (sp) là tổng enthalpy tạo thành ở điều kiện chuẩn của chất đầu và sản phẩm của phản ứng.
(sp) là tổng enthalpy tạo thành ở điều kiện chuẩn của chất đầu và sản phẩm của phản ứng.
Xét phương trình nhiệt hóa học:
2H2 (g) + O2 (g) ⟶ 2H2O (g) 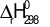 = − 483,64 kJ
= − 483,64 kJ
Ta thấy: 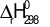 = − 483,64 kJ < 0
= − 483,64 kJ < 0
Nên 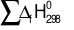 (sp) –
(sp) – 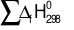 (cđ) < 0
(cđ) < 0
Do đó: 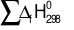 (sp) <
(sp) <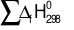 (cđ) hay
(cđ) hay 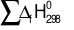 (cđ) >
(cđ) >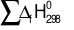 (sp).
(sp).

 2H2O (g)
2H2O (g)