Giải Hóa 10 trang 73 Chân trời sáng tạo
Haylamdo biên soạn và sưu tầm lời giải Hóa 10 trang 73 sách Chân trời sáng tạo. Với lời giải chi tiết nhất hy vọng sẽ giúp học sinh dễ dàng nắm được cách làm bài tập Hóa học 10.
Giải Hóa học 10 trang 73 Chân trời sáng tạo
Câu hỏi 2 trang 73 Hóa học 10: Quan sát Hình 12.2a hydrogen cháy trong chlorine với ngọn lửa sáng, tạo hợp chất hydrogen chloride (HCl). Nếu cặp electron chung trong hợp chất cộng hóa trị HCl lệch hẳn về phía nguyên tử Cl (Hình 12.2b), hãy xác định điện tích của các nguyên tử trong phân tử HCl
Lời giải:
Giả định nếu cặp electron chung trong hợp chất cộng hóa trị HCl lệch hẳn về phía nguyên tử Cl khi đó có thể coi Cl nhận 1 electron và H nhường 1 electron
⇒ Cl mang điện tích -1 và H mang điện tích +1
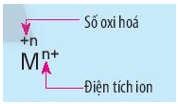
Câu hỏi 3 trang 73 Hóa học 10: Nêu điểm khác nhau giữa kí hiệu oxi hóa và kí hiệu điện tích của ion M trong hình sau:
Lời giải:
Kí hiệu số oxi hóa: Dấu viết trước, số viết sau.
Kí hiệu điện tích ion: số viết trước, dấu viết sau.
Câu hỏi 4 trang 73 Hóa học 10: Dự đoán số oxi hóa của các nguyên tử trong nhóm IA, IIA, IIIA trong các hợp chất. Giải thích
Lời giải:
- Các nguyên tử nguyên tố nhóm IA đều có 1 electron lớp ngoài cùng, trong quá trình hình thành liên kết hóa học có xu hướng nhường đi 1 electron này để đạt được cấu hình electron bền vững của khí hiếm.
⇒ Các nguyên tử trong nhóm IA có số oxi hóa là +1
- Các nguyên tử nguyên tố nhóm IIA đều có 2 electron lớp ngoài cùng, trong quá trình hình thành liên kết hóa học có xu hướng nhường đi 2 electron này để đạt được cấu hình electron bền vững của khí hiếm.
⇒ Các nguyên tử trong nhóm IIA có số oxi hóa là +2
- Các nguyên tử nguyên tố nhóm IIIA đều có 3 electron lớp ngoài cùng, trong quá trình hình thành liên kết hóa học có xu hướng nhường đi 3 electron này để đạt được cấu hình electron bền vững của khí hiếm.
⇒ Các nguyên tử trong nhóm IIIA có số oxi hóa là +3.
Luyện tập trang 73 Hóa học 10: Hãy xác định số oxi hóa của các nguyên tử trong các đơn chất, hợp chất và ion sau: Zn, H2, Cl‑, O2-, S2-, HSO4-, Na2S2O3, KNO3
Lời giải:
- Số oxi hóa của nguyên tử trong các đơn chất bằng 0
⇒ Số oxi hóa:
- Đối với ion đơn nguyên tử, số oxi hóa của nguyên tử trong ion bằng điện tích của ion đó.
⇒ Số oxi hóa của nguyên tử Cl, O, S trong Cl‑, O2-, S2-lần lượt bằng -1; -2; -2.
- Đối với ion đa nguyên tử, tổng số oxi hóa của các nguyên tử bằng điện tích của ion đó.
- Trong đa số các hợp chất, số oxi hóa của hydrogen bằng +1, số oxi hóa của oxygen bằng -2.
⇒ Xét ion HSO4-
+ Số oxi hóa của H là +1, của O là -2
+ Số oxi hóa của S là x ta có: 1.(+1) + 1.x + 4.(-2) = -1 ⇒ x = +6
- Trong một phân tử, tổng số oxi hóa của các nguyên tử bằng 0.
- Kim loại kiềm (nhóm IA) luôn có số oxi hóa +1.
⇒ Xét phân tử Na2S2O3
+ Số oxi hóa của Na là +1
+ Số oxi hóa của O là -2
+ Số oxi hóa của S là x ta có: 2.(+1) + 2.x + 3.(-2) = 0 ⇒ x = +2
Xét phân tử KNO3
+ Số oxi hóa của K là +1
+ Số oxi hóa của O là -2
+ Số oxi hóa của N là x ta có: 1.(+1) + 1.x + 3.(-2) = 0 ⇒ x = +5