Giải Hóa 10 trang 84 Chân trời sáng tạo
Haylamdo biên soạn và sưu tầm lời giải Hóa 10 trang 84 sách Chân trời sáng tạo. Với lời giải chi tiết nhất hy vọng sẽ giúp học sinh dễ dàng nắm được cách làm bài tập Hóa học 10.
Giải Hóa học 10 trang 84 Chân trời sáng tạo
Câu hỏi 8 trang 84 Hóa học 10: Phân biệt enthalpy tạo thành của một chất và biến thiên enthalpy của phản ứng. Lấy ví dụ minh họa
Lời giải:
Enthalpy tạo thành của một chất |
Enthalpy của phản ứng |
|
- Chỉ tạo thành 1 mol chất. - Các chất tham gia phải ở dạng đơn chất bền nhất. |
- Sản phẩm có thể là 1 hay nhiều chất. - Các chất tham gia có thể ở dạng đơn chất hoặc hợp chất. |
|
Ví dụ: C (graphite) + O2(g) CO2 ∆ f(CO2, g) = -393,50 kJ/mol Carbon dạng graphite, oxygen dạng phân tử khí là các dạng đơn chất bền nhất của carbon và oxygen. |
Ví dụ: C2H5OH(l) + 3O2(g) 2CO2(g) + 3H2O(l) ∆r = -1366,89 kJ |
Câu hỏi 9 trang 84 Hóa học 10: Cho phản ứng sau:
S(s) + O2(g) SO2(g)
∆ f(SO2, g) = -296,80 kJ/mol
Cho biết ý nghĩa của giá trị ∆ f(SO2, g)
Lời giải:
∆ f(SO2, g) = -296,80 kJ/mol là lượng nhiệt tỏa ra khi tạo ra 1 mol SO2(g) từ các đơn chất ở trạng thái bền ở điều kiện chuẩn (sulfur ở trạng thái rắn, oxygen dạng phân tử khí chính là các dạng đơn chất bền nhất của sulfur và oxygen).
Câu hỏi 10 trang 84 Hóa học 10: Hợp chất SO2(g) bền hơn hay kém bền hơn về mặt năng lượng so với các đơn chất bền S(s) và O2(g)
Lời giải:
∆ f(SO2, g) = -296,80 kJ/mol < 0
⇒ Hợp chất SO2(g) bền hơn về mặt năng lượng so với các đơn chất bền S(s) và O2(g).
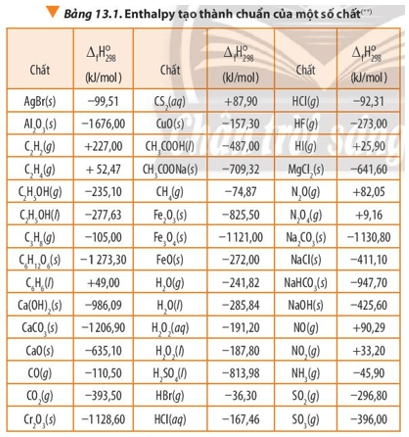
Câu hỏi 11 trang 84 Hóa học 10: Từ Bảng 13.1 hãy liệt kê các phản ứng có enthalpy tạo thành dương (lấy nhiệt từ môi trường)
Lời giải:
Các phản ứng có enthalpy tạo thành dương (lấy nhiệt từ môi trường):
Phản ứng tạo thành các chất: C2H2(g), C2H4(g), C6H6(l), CS2(aq), HI(g), N2O(g), N2O4(g), NO(g), NO2(g).
Luyện tập trang 84 Hóa học 10: Em hãy xác định enthalpy tạo thành theo đơn vị (kcal) của các chất sau: Fe2O3(s), NO(g), H2O(g), C2H5OH(l). Cho biết 1J = 0,239 cal
Lời giải:
1J = 0,239 cal
⇒ 1 kJ = 0,239 kcal
∆ f(Fe2O3, s) = -825,50 kJ/mol = -825,50 . 0,239 kcal/mol = -197,29 kcal/mol
∆ f(NO, g) = +90,29 kJ/mol = +21,58 kcal/mol
∆ f(H2O, g) = -241,82 kJ/mol = -57,79 kcal/mol
∆ f(C2H5OH, l) = -277,63 kJ/mol = -66,35 kcal/mol