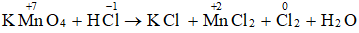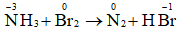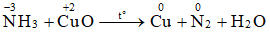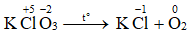Lập phương trình hóa học của các phản ứng oxi hóa - khử sau
Giải Hóa 10 Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
Haylamdo biên soạn và sưu tầm lời giải Luyện tập trang 77 Hóa học 10 trong Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống sách Chân trời sáng tạo, lời giải chi tiết sẽ giúp học sinh biết cách làm bài tập Hóa học 10.
Luyện tập trang 77 Hóa học 10: Lập phương trình hóa học của các phản ứng oxi hóa - khử sau, xác định vai trò của các chất tham gia phản ứng.
KMnO4 + HCl → KCl + MnCl2 + Cl↑ + H2O (1)
NH3 + Br2 → N2 + HBr (2)
NH3 + CuO Cu + N2 + H2O (3)
FeS2 + O2 Fe2O3 + SO2 (4)
KClO3 KCl + O2↑ (5)
Lời giải:
KMnO4 + HCl → KCl + MnCl2 + Cl↑ + H2O (1)
Bước 1:
Chất khử: HCl
Chất oxi hóa: KMnO4
Bước 2:
Quá trình oxi hóa:
Quá trình khử:
Bước 3:
Bước 4:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
NH3 + Br2 → N2 + HBr (2)
Bước 1:
Chất khử: NH3
Chất oxi hóa: Br2
Bước 2:
Quá trình oxi hóa:
Quá trình khử:
Bước 3:
Bước 4:
2NH3 + 3Br2 → N2 + 6HBr
NH3 + CuO Cu + N2 + H2O (3)
Bước 1:
Chất khử: NH3
Chất oxi hóa: CuO
Bước 2:
Quá trình oxi hóa:
Quá trình khử:
Bước 3:
Bước 4:
2NH3 + 3CuO 3Cu + N2 + 3H2O
FeS2 + O2 Fe2O3 + SO2 (4)
Bước 1:
Chất khử: FeS2
Chất oxi hóa: O2
Bước 2: Quá trình oxi hóa:
Quá trình khử:
Bước 3:
Bước 4:
4FeS2 + 11O2 2Fe2O3 + 8SO2
KClO3 KCl + O2↑ (5)
Bước 1:
KClO3 vừa là chất khử, vừa là chất oxi hóa
Bước 2:
Quá trình oxi hóa:
Quá trình khử:
Bước 3:
Bước 4:
2KClO3 2KCl + 3O2↑