Xác định nồng độ của dung dịch FeSO4 bằng dung dịch KMnO4 (dung dịch thuốc tím)
Giải Hóa 12 Bài 20: Sơ lược về kim lại chuyển tiếp dãy thứ nhất - Cánh diều
Thí nghiệm 1 trang 138 Hóa học 12: Xác định nồng độ của dung dịch FeSO4 bằng dung dịch KMnO4 (dung dịch thuốc tím)
Chuẩn bị:
- Hoá chất: Dung dịch thuốc tím KMnO4 có nồng độ chính xác 0,02 M, dung dịch FeSO4 có nồng độ khoảng 0,1 M; dung dịch H2SO4 20%.
- Dụng cụ : Burette loại 25 mL, bình tam giác loại 100 mL.
Tiến hành:
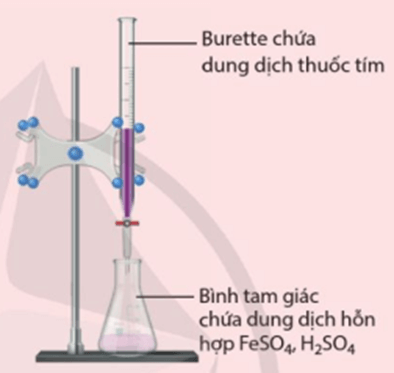
Hình 20.1. Bộ dụng cụ thí nghiệm chuẩn độ muối FeSO4 trong môi trường acid bằng dung dịch thuốc tím
- Lắp bộ dụng cụ như Hình 20.1. Cho dung dịch thuốc tím vào burette đến vạch 0, đồng thời bảo đảm không còn bọt khí trong burette. Cho 10 mL dung dịch FeSO4 và 5 mL dung dịch H2SO4 20% vào bình tam giác.
- Mở khoá để nhỏ từ từ từng giọt dung dịch thuốc tím vào bình tam giác, đồng thời lắc đều bình.
- Tiếp tục nhỏ dung dịch thuốc tím (vẫn duy trì lắc đều bình) tới khi dung dịch trong bình tam giác xuất hiện màu hồng nhạt bởi một giọt thuốc tím dư, không mất màu trong khoảng 20 giây thì kết thúc chuẩn độ (khoá burette).
- Ghi lại thể tích dung dịch thuốc tím đã dùng.
Lặp lại thí nghiệm ít nhất hai lần nữa.
Yêu cầu: Xác định nồng độ của dung dịch FeSO4. Biết phương trình hoá học của phản ứng diễn ra trong quá trình chuẩn độ là:
5Fe2+(aq) + (aq) + 8H+(aq) →5Fe3+(aq) + Mn2+(aq) + 4H₂O(1)
Lời giải:
Gọi thể tích dung dịch KMnO4 đã dùng ở các lần đo lần lượt là V1, V2, …, Vn
Ta có thể tích trung bình của dung dịch KMnO4 là:
Theo phương trình chuẩn độ, ta có:
⇒
Thay số liệu vào công thức trên ta xác định được nồng độ của dung dịch FeSO4.
Lời giải Hóa 12 Bài 20: Sơ lược về kim lại chuyển tiếp dãy thứ nhất hay khác:
Mở đầu trang 135 Hóa học 12: Kim loại chuyển tiếp dãy thứ nhất gồm 9 nguyên tố từ Sc ....
Câu hỏi 1 trang 136 Hóa học 12: Dựa vào Bảng 20.1, giải thích vì sao nhiều kim loại chuyển tiếp ....
Thí nghiệm 2 trang 138 Hóa học 12: Kiểm tra sự có mặt của cation Cu2+ hoặc Fe3+ trong dung dịch ....
Bài 3 trang 141 Hóa học 12: Một mẫu chất có thành phần chính là muối Mohr ....