Giải Hóa học 12 trang 122 Kết nối tri thức
Haylamdo biên soạn và sưu tầm lời giải bài tập Hóa học 12 trang 122 trong Bài 25: Nguyên tố nhóm IIA Hóa học 12 Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời các câu hỏi & làm bài tập Hóa 12 trang 122.
Giải Hóa học 12 trang 122 Kết nối tri thức
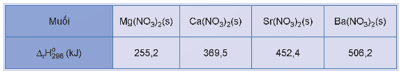
Hoạt động trang 122 Hóa học 12: Biến thiên enthalpy chuẩn của phản ứng nhiệt phân các muối nitrate của kim loại nhóm IIA:
cho trong bảng sau:
Thực hiện yêu cầu sau:
Dựa vào biến thiên enthalpy chuẩn của phản ứng, dự đoán xu hướng biến đổi độ bền nhiệt của muối nitrate của kim loại nhóm IIA.
Lời giải:
Dựa vào biến thiên enthalpy chuẩn của phản ứng, dự đoán độ bền nhiệt của các muối tăng dần theo thứ tự: Mg(NO3)2, Ca(NO3)2, Sr(NO3)2, Ba(NO3)2.
Hoạt động thí nghiệm trang 122 Hóa học 12: Phân biệt từng ion riêng rẽ Ca2+, Ba2+, SO42-, CO32- có trong dung dịch
Chuẩn bị:
Hoá chất: các dung dịch: CaCl2 1 M, BaCl2 1 M, Na2SO4 1 M, Na2CO3 1M, HCl 2 M. Dụng cụ: ống nghiệm, giá ống nghiệm.
Tiến hành:
1. Nhận biết từng ion riêng rẽ
Cho vào ống nghiệm (1) khoảng 1 mL dung dịch CaCl2 1 M, ống nghiệm (2) khoảng 1 mL dung dịch BaCl2 1 M, ống nghiệm (3) khoảng 1 mL Na2SO4 1 M.
- Nhỏ từ từ từng giọt dung dịch Na2SO4 1 M vào mỗi ống nghiệm (1) và ống nghiệm (2); nhỏ vài giọt dung dịch BaCl2 1 M vào ống nghiệm (3).
Chú ý: BaCl2 độc, cần tuân thủ quy tắc an toàn trong phòng thí nghiệm.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
1. Viết phương trình hoá học của các phản ứng xảy ra trong mỗi ống nghiệm.
2. Ở ống nghiệm (1) và (2), ống nào tạo kết tủa nhanh hơn? Nhiều hơn?
2. Nhận biết ion
- Cho khoảng 1 mL dung dịch Na2CO3 1 M vào ống nghiệm, thêm tiếp khoảng 1 mL dung dịch CaCl2 1 M, lắc đều.
- Thêm tiếp 2 mL dung dịch HCl 2 M vào ống nghiệm, lắc đều.
Quan sát hiện tượng xảy ra và thực hiện các yêu cầu sau:
1. Viết phương trình hoá học của các phản ứng xảy ra trong thí nghiệm.
2. Nêu các hiện tượng xảy ra và giải thích.
Lời giải:
1. Nhận biết từng ion riêng rẽ
1. Phương trình hoá học của các phản ứng xảy ra trong mỗi ống nghiệm.
Ống nghiệm 1: CaCl2 + Na2SO4 → CaSO4 + 2NaCl.
Ống nghiệm 2: BaCl2 + Na2SO4 → BaSO4 + 2NaCl.
Ống nghiệm 3: Na2SO4 + BaCl2 → BaSO4 + 2NaCl.
2. Ở ống nghiệm (1) và (2), ống nghiệm (2) tạo kết tủa nhanh hơn, nhiều hơn do độ tan tan của BaSO4 là 0,0028 g/100 g nước còn độ tan của CaSO4 là 0,2 g/100 g nước.
2. Nhận biết ion
1. Phương trình hoá học của các phản ứng xảy ra trong thí nghiệm:
Na2CO3(aq) + CaCl2(aq) → CaCO3(s) + 2NaCl(aq)
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + CO2(g) + H2O(l)
2.
|
Bước tiến hành |
Hiện tượng |
Giải thích |
|
- Cho khoảng 1 mL dung dịch Na2CO3 1 M vào ống nghiệm, thêm tiếp khoảng 1 mL dung dịch CaCl2 1 M, lắc đều. |
Xuất hiện kết tủa trắng. |
Na2CO3 phản ứng với CaCl2 sinh ra chất kết tủa là CaCO3 có màu trắng. Na2CO3(aq) + CaCl2(aq) → CaCO3(s) + 2NaCl(aq) |
|
- Thêm tiếp 2 mL dung dịch HCl 2 M vào ống nghiệm, lắc đều. |
Kết tủa tan dần, có khí thoát ra. |
Tiếp tục thêm HCl vào ống nghiệm, HCl phản ứng với CaCO3 tạo thành muối tan là CaCl2 và giải phóng khí CO2. CaCO3(s) + 2HCl(aq) → CaCl2(aq) + CO2(g) + H2O(l) |
Lời giải Hóa 12 Bài 25: Nguyên tố nhóm IIA hay khác: