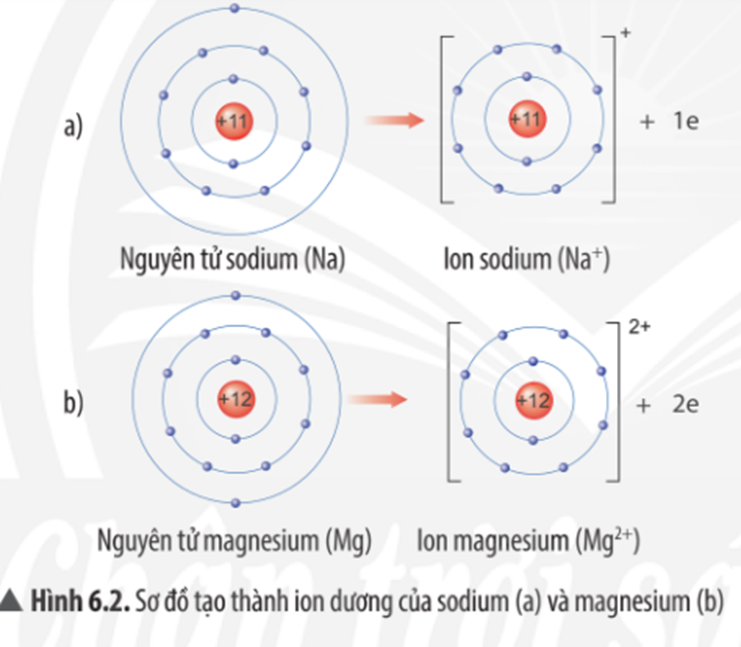
Quan sát Hình 6.2, em hãy mô tả sự tạo thành ion sodium, ion magnesium
Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học
Haylamdo biên soạn và sưu tầm lời giải Câu hỏi thảo luận 2 trang 38 KHTN lớp 7 trong Bài 6: Giới thiệu về liên kết hóa học .Với lời giải được biên soạn chi tiết sẽ giúp học sinh biết cách làm bài tập KHTN 7.
Câu hỏi thảo luận 2 trang 38 KHTN lớp 7: Câu hỏi thảo luận 2 trang 38 SGK Khoa học tự nhiên 7: Quan sát Hình 6.2, em hãy mô tả sự tạo thành ion sodium, ion magnesium. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
Trả lời:
Mô tả sự tạo thành ion sodium, ion magnesium:
- Nguyên tử sodium (Na) nhường đi 1 electron ở lớp vỏ ngoài cùng để trở thành ion sodium mang điện tích dương, kí hiệu Na+
- Nguyên tử magnesium (Mg) nhường đi 2 electron ở lớp vỏ ngoài cùng để trở thành ion magnesium mang điện tích dương, kí hiệu Mg2+
Nhận xét:
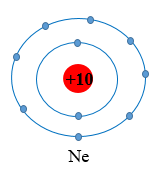
- Các ion này đều có 8 electron lớp ngoài cùng.
- Sự phân bố electron của ion sodium (Na+) và ion magnesium (Mg2+) đều giống với sự phân bố electron của nguyên tử khí hiếm neon (Ne).