Giải SBT Hóa học 10 trang 19 Cánh diều
Haylamdo biên soạn và sưu tầm lời giải SBT Hóa học 10 trang 19 trong Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học sách Cánh diều. Với lời giải chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập SBT Hóa học 10.
Giải SBT Hóa học 10 trang 19 Cánh diều
Bài 6.9 trang 19 sách bài tập Hóa học 10: Cho cấu hình electron các nguyên tố sau đây: Na: [Ne]3s1, Cr: [Ar]3d54s1, Br: [Ar]3d104s24p5, F: 1s22s22p5, Cu: [Ar]3d104s1. Số nguyên tố thuộc khối s, p, d trong các nguyên tố trên lần lượt là:
A. 2, 1, 2.
B. 1, 2, 2.
C. 1, 1, 3.
D. Không xác định được.
Lời giải:
Đáp án đúng là: B
- Nguyên tố s là nguyên tố nhóm A mà nguyên tử có cấu hình electron lớp ngoài cùng là ns1÷2. Nguyên tố thuộc khối s: Na: [Ne]3s1.
- Nguyên tố p là nguyên tố nhóm A mà nguyên tử có cấu hình electron lớp ngoài cùng là ns2np1÷6. Nguyên tố thuộc khối p: Br: [Ar]3d104s24p5 và F: 1s22s22p5.
- Nguyên tố d là nguyên tố nhóm B mà nguyên tử có cấu hình electron phân lớp ngoài cùng và phân lớp sát lớp ngoài cùng là (n – 1)d1÷10ns1÷2. Nguyên tố thuộc khối d: Cr: [Ar]3d54s1 và Cu: [Ar]3d104s1.
Bài 6.10 trang 19 sách bài tập Hóa học 10: Những nguyên tố được xếp riêng bên dưới bảng tuần hoàn thuộc khối nguyên tố nào?
A. s.
B. p.
C. d.
D. f.
Lời giải:
Đáp án đúng là: D
Các nguyên tố f được xếp riêng bên dưới bảng tuần hoàn.
Bài 6.11 trang 19 sách bài tập Hóa học 10: Hãy giải thích vì sao khối nguyên tố s trong bảng tuần hoàn chỉ có hai cột trong khi khối nguyên tố p có sáu cột.
Lời giải:
- Khối s là các nguyên tố có cấu hình electron lớp ngoài cùng là ns1÷2, tức là cấu hình electron đang hoàn thành phân lớp s. Phân lớp s chỉ chứa tối đa 2 electron, nên khối s chỉ có 2 cột, ứng với hai cấu hình electron lớp ngoài cùng là ns1 và ns2.
- Tương tự, khối p là các nguyên tố mà cấu hình electron lớp ngoài cùng là ns2np1÷6, tức là cấu hình electron đang hoàn thành phân lớp p. Phân lớp p chứa tối đa 6 electron nên khối p có 6 cột, ứng với 6 cấu hình electron lớp ngoài cùng: ns2np1; ns2np2; ns2np3; ns2np4; ns2np5; ns2np6.
Bài 6.12 trang 19 sách bài tập Hóa học 10: Vì sao số lượng các nguyên tố trong các chu kì của bảng tuần hoàn có sự khác biệt: chu kì 1 có 2 nguyên tố, mỗi chu kì 2 và 3 có 8 nguyên tố; chu kì 4 có 18 nguyên tố?
Lời giải:
Vì chu kì là tập hợp các nguyên tố có cùng số lớp electron nên số lượng các ô trong một chu kì bằng số lượng electron trong một lớp.
Ở lớp thứ nhất chỉ chứa tối đa 2 electron (vào phân lớp 1s); ở lớp thứ hai chỉ chứa tối đa 8 electron (vào phân lớp 2s, 2p) nên chu kì 1 có 2 nguyên tố và chu kì 2 có 8 nguyên tố.
Với chu kì 3, sau khi điền đầy đủ phân lớp 3s và 3p (8 electron ứng với số lượng 8 nguyên tố), thì chuyển sang điền electron vào phân lớp 4s chứ không phải 3d, nên chu kì 3 chỉ có 8 nguyên tố.
Chu kì 4 sẽ hoàn thiện các phân lớp 4s, 4p (tổng số electron tối đa trên các phân lớp này là 8 electron) và cả phân lớp 3d (tối đa 10 electron) nên chu kì 4 có 18 nguyên tố.
Bài 6.13 trang 19 sách bài tập Hóa học 10: Calcium (Ca) là nguyên tố kim loại chiếm khối lượng nhiều nhất trong cơ thể con người. Răng và xương là các bộ phận chứa nhiều calcium nhất. Số hiệu nguyên tử của Ca là 20. Hãy xác định vị trí của calcium trong bảng tuần hoàn.
Lời giải:
Cấu hình electron Ca (Z = 20): 1s22s22p63s23p64s2. Vậy Ca ở:
+ Ô thứ 20 (do Z = 20)
+ Chu kì 4 (do có 4 lớp electron)
+ Nhóm IIA (do nguyên tố s, 2 electron ở lớp ngoài cùng).
Bài 6.14 trang 19 sách bài tập Hóa học 10: Em cần giải một mật mã sử dụng các kí hiệu nguyên tố để xác định các chữ cái trong mật mã. Quy tắc của mật mã như sau:
(1) Cho một dãy số, trong đó mỗi số là tổng của số hiệu nguyên tử và số lớp electron của một nguyên tử ứng với một nguyên tố hoá học.
(2) Chữ cái đầu tiên trong kí hiệu hoá học của mỗi nguyên tố thu được từ việc giải mã dãy số ở quy tắc thứ nhất sẽ tương ứng với một chữ cái trong mật mã.
Em hãy thử giải mật mã theo quy tắc trên với dãy số sau: 8, 2, 69, 29, 58, 19, 26, 42, 76 (các chữ cái của mật mã sắp xếp theo đúng thứ tự tương ứng với các con số).
Lời giải:
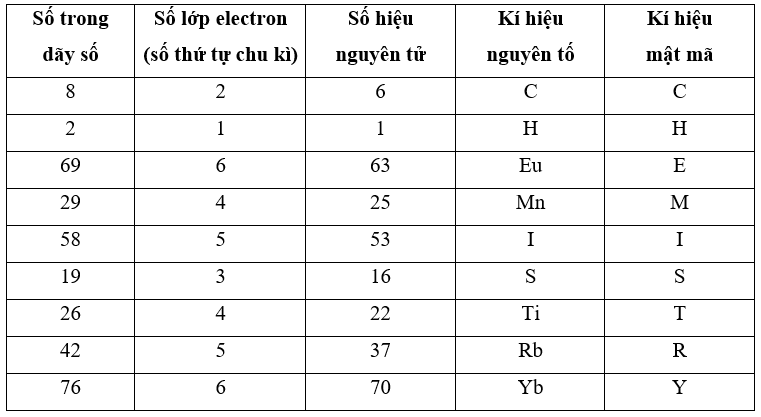
Dựa vào bảng tuần hoàn ta có thể xác định được số thứ tự của chu kì của nguyên tố đó, cũng tức là số lớp electron chỉ có thể nằm trong khoảng từ 1 đến 7. Kết quả thu được như sau:
Mật mã: CHEMISTRY
Lời giải sách bài tập Hóa học lớp 10 Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học Cánh diều hay khác: