Giải SBT Hóa học 10 trang 43 Cánh diều
Haylamdo biên soạn và sưu tầm lời giải SBT Hóa học 10 trang 43 trong Bài 14: Phản ứng hóa học và enthalpy sách Cánh diều. Với lời giải chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập SBT Hóa học 10.
Giải SBT Hóa học 10 trang 43 Cánh diều
Bài 14.9 trang 43 sách bài tập Hóa học 10: Phản ứng phân hủy 1 mol H2O (g) ở điều kiện tiêu chuẩn:
cần cung cấp một nhiệt lượng là 241,8 kJ.
Điền vào chỗ trống trong các phát biểu dưới đây:
a) Phản ứng (1) là phản ứng …… nhiệt.
b) Nhiệt tạo thành chuẩn của H2O (g) là ……..
c) Biến thiên enthalpy chuẩn của phản ứng 2H2(g) + O2(g) → 2H2O(g) là …….
d) Biến thiên enthalpy chuẩn của phản ứng (1) là ………
Lời giải:
a) Phản ứng (1) là phản ứng thu nhiệt.
b) Nhiệt tạo thành chuẩn của H2O (g) là -241,8 kJ mol-1.
c) Biến thiên enthalpy chuẩn của phản ứng 2H2(g) + O2(g) → 2H2O(g) là -483,6 kJ.
d) Biến thiên enthalpy chuẩn của phản ứng (1) là 248,1 kJ.
Bài 14.10 trang 43 sách bài tập Hóa học 10: Phương trình hóa học nào dưới đây biểu thị enthalpy tạo thành chuẩn của CO(g)?
A. 2C(than chì) + O2(g) → 2CO(g)
B. C(than chì) + O(g) → CO(g)
C. C(than chì) +
D. C(than chì) + CO2(g) → 2CO(g)
E. CO(g) → C(than chì) + O(g).
Lời giải:
Đáp án đúng là: C
Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất là lượng nhiệt kèm theo của phản ứng tạo thành 1 mol chất đó từ các đơn chất dạng bền nhất trong điều kiện chuẩn.
Vậy phương trình biểu thị enthalpy tạo thành chuẩn của CO(g) là:
C(than chì) +
Bài 14.11 trang 43 sách bài tập Hóa học 10: Khi pha loãng 100 mL H2SO4 đặc bằng nước thấy cốc đựng dung dịch nóng lên. Vậy quá trình pha loãng H2SO4 đặc là quá trình thu nhiệt hay tỏa nhiệt?
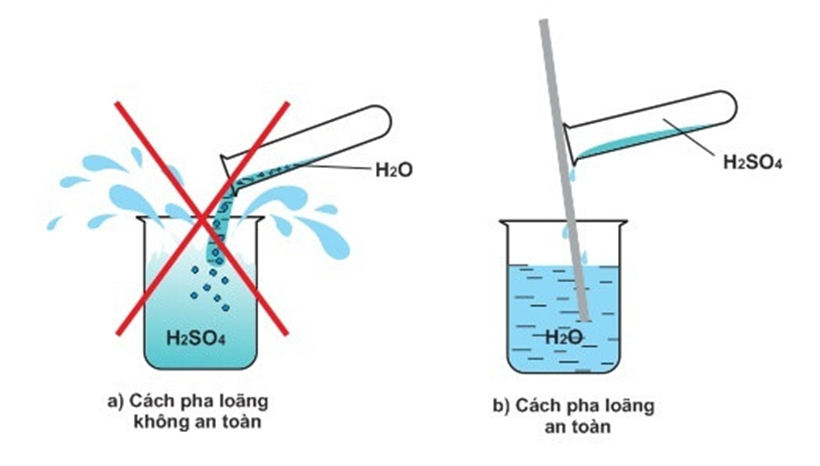
Theo em, khi pha loãng H2SO4 đặc nên cho từ từ H2SO4 đặc vào nước hay ngược lại? Vì sao?
Lời giải:
Khi pha loãng 100 mL H2SO4 đặc bằng nước thấy cốc đựng dung dịch nóng lên. Vậy quá trình pha loãng H2SO4 đặc là quá trình tỏa nhiệt.
Để pha loãng H2SO4 đặc an toàn cần cho từ từ H2SO4 đặc vào nước và khuấy nhẹ bằng đũa thủy tinh. Tuyệt đối không làm ngược lại vì phản ứng tỏa nhiệt mạnh, làm nước sôi đột ngột kéo theo những giọt acid bắn ra ngoài gây nguy hiểm.
Bài 14.12 trang 43 sách bài tập Hóa học 10: Nhiệt tỏa ra khi đốt cháy 1 gam một mẫu than là 23,0 kJ. Giả thiết rằng toàn bộ lượng nhiệt của quá trình đốt than tỏa ra đều dùng để làm nóng nước, không có sự thất thoát nhiệt, hãy tính lượng than cần phải đốt để làm nóng 500 gam nước từ 20oC tới 90oC. Biết để làm nóng 1 mol nước thêm 1oC cần một nhiệt lượng là 75,4 J.
Lời giải:
Lượng nhiệt cần để làm nóng 500 gam nước từ 20oC tới 90oC là:
Lượng than cần phải đốt là:
Lời giải sách bài tập Hóa học lớp 10 Bài 14: Phản ứng hóa học và enthalpy Cánh diều hay khác: