Oxide ứng với hóa trị cao nhất của một nguyên tố có công thức thực nghiệm là R2O5. Oxide này là một chất hút nước mạnh
Giải SBT Hóa 10 Kết nối tri thức Bài 9: Ôn tập chương 2
Haylamdo biên soạn và sưu tầm lời giải Bài 9.15 trang 26 SBT Hóa học 10 trong Bài 9: Ôn tập chương 2 sách Kết nối tri thức. Với lời giải chi tiết nhất hy vọng sẽ giúp học sinh dễ dàng nắm được cách làm bài tập Sách bài tập Hóa 10.
Bài 9.15 trang 26 SBT Hóa học 10: Oxide ứng với hóa trị cao nhất của một nguyên tố có công thức thực nghiệm là R2O5. Oxide này là một chất hút nước mạnh, được sử dụng trong tổng hợp chất hữu cơ. Khả năng hút ẩm của nó đủ mạnh để chuyển nhiều acid vô cơ thành các alhydrite (oxide tương ứng) của chúng. Hợp chất khí của R với hydrogen có chứa 8,82% khối lượng hydrogen và là chất khí không màu, rất độc, kém bền, sinh ra trong quá trình phân hủy xác động thực vật.
a) Nêu vị trí của R trong bảng tuần hoàn.
b) Viết cấu hình electron theo ô orbital của nguyên tử R.
c) Nêu một số tính chất hóa học cơ bản của R và hợp chất.
Lời giải:
a) Hợp chất khí của R với hydrogen có dạng RH3.
Ta có: ⇒ R = 31. R là P (phosphorus)
Vị trí trong bảng tuần hoàn của R: ô số 15, chu kì 3, nhóm VA.
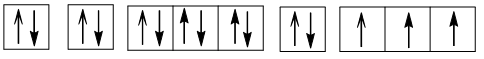
b) Cấu hình electron của R: 1s22s22p63s23p3
c) - Tính chất đơn chất: nguyên tố P là phi kim trung bình:
+ Phản ứng với oxygen tạo oxide.
+ Phản ứng với chlorine tạo phosphorus chloride.
+ Phản ứng với kim loại tạo phosphide.
- Tính chất hợp chất: P2O5 là acidic oxide phản ứng với nước tạo hydroxide tương ứng H3PO4 là acid.