Nếu tăng áp suất của hệ phản ứng và giữ nhiệt độ không đổi
Sách bài tập Hóa học 11 Bài 1: Khái niệm về cân bằng hóa học - Chân trời sáng tạo
Trong quy trình sản xuất sulfuric acid (H2SO4) có giai đoạn dùng dung dịch H2SO4 98% hấp thụ sulfur trioxide (SO3) thu được oleum (H2SO4.nSO3). Sulfur trioxide được tạo thành bằng cách oxi hoá sulfur dioxide bằng oxygen hoặc lượng dư không khí ở nhiệt độ 450 °C - 500 °C, chất xúc tác vanadium(V) oxide (V2O5) theo phương trình hoá học:
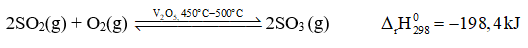
Bài 1.10 trang 6 Sách bài tập Hóa học 11: Nếu tăng áp suất của hệ phản ứng và giữ nhiệt độ không đổi thì cân bằng của hệ sẽ chuyển dịch theo chiều nào?
Lời giải:
Cân bằng chuyển dịch theo chiều thuận (chiều làm giảm áp suất của hệ phản ứng tức chiều làm giảm số mol khí).
Lời giải SBT Hóa 11 Bài 1: Khái niệm về cân bằng hóa học hay khác:
Bài 1.3 trang 5 Sách bài tập Hóa học 11: Cân bằng hoá học sẽ chuyển dịch theo chiều nào khi ....
Bài 1.6 trang 6 Sách bài tập Hóa học 11: Cân bằng hoá học sẽ chuyển dịch theo chiều nào khi ....
Bài 1.8 trang 6 Sách bài tập Hóa học 11: Nồng độ ban đầu của SO2 và O2 tương ứng là 4 M và 2 M ....
Bài 1.15 trang 7 Sách bài tập Hóa học 11: Cho vào bình kín (dung tích 1 L) 1 mol H2 và 1 mol I2 ....

