Với cách viết công thức cấu tạo gồm 3 liên kết đôi xen lẫn 3 liên kết đơn trong vòng 6 cạnh
Với cách viết công thức cấu tạo gồm 3 liên kết đôi xen lẫn 3 liên kết đơn trong vòng 6 cạnh, có thể gọi tên benzene là cyclohexe-1,3,5-triene được không? Vì sao?
Sách bài tập Hóa học 11 Bài 14: Arene (Hydrocarbon thơm) - Chân trời sáng tạo
Bài 14.22 trang 66 Sách bài tập Hóa học 11: Với cách viết công thức cấu tạo gồm 3 liên kết đôi xen lẫn 3 liên kết đơn trong vòng 6 cạnh, có thể gọi tên benzene là cyclohexe-1,3,5-triene được không? Vì sao?
Lời giải:
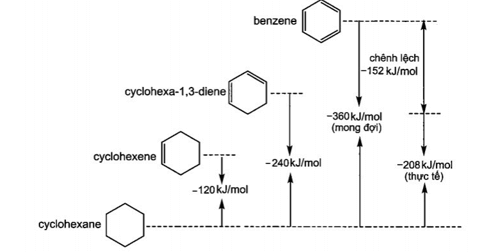
Biến thiên enthalpy của quá trình hydrogen hoá cyclohexene và cyclohexa-1,3-diene thành cyclohexane lần lượt là -120 kJ/mol và -240 kJ/mol, do đó biến thiên enthalpy của quá trình hydrogen hoá benzene được mong đợi sẽ là 3×120 = -360 (kJ/mol). Tuy nhiên thực tế biến thiên enthalpy của quá trình hydrogen hoá benzene chỉ là -208 (kJ/mol) (xem sơ đồ minh hoạ), cho thấy phân tử benzene không thể chứa ba liên kết đôi. Nói khác đi, các liên kết π được định vị trên toàn bô vòng benzene, nên không thể gọi benzene là cyclohexa-1,3,5-trien.
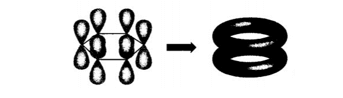
Sự hình thành liên kết σ và hệ liên hợp π trong phân tử benzene
Năm 1929, nhà nữ bác học người Anh, Kathleen Lonsdale (1903 - 1971), đã sử dụng phương pháp phân tích nhiễu xạ tia X để chỉ ra rằng tất cả độ dài liên kết C-C trong benzene là giống hệt nhau. Khoảng cách này nhỏ hơn độ dài của liên kết C-C và dài hơn của liên kết C=C. Điều này cho thấy ba liên kết π trong phân tử benzene phải được trải đều trên toàn bộ vòng benzene, cũng có nghĩa benzene không có cấu trúc của cyclohexa-1,3,5-triene.
Lời giải SBT Hóa 11 Bài 14: Arene (Hydrocarbon thơm) hay khác:
Bài 14.4 trang 60 Sách bài tập Hóa học 11: Công thức phân tử của anthracene là....
Bài 14.5 trang 60 Sách bài tập Hóa học 11: Số liên kết π trong phân tử anthracene là bao nhiêu?....
Bài 14.7 trang 61 Sách bài tập Hóa học 11: Gọi tên arene sau theo danh pháp thay thế ....