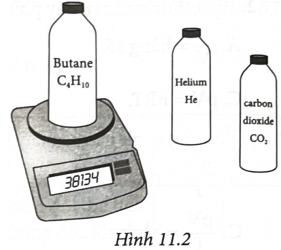
Có ba chai thuỷ tinh giống nhau khối lượng và dung tích bằng nhau đựng các chất khí khác nhau
Có ba chai thuỷ tinh giống nhau (khối lượng và dung tích bằng nhau) đựng các chất khí khác nhau (He, CH, CO) ở cùng nhiệt độ 20 °C và áp suất 1,913.10 Pa. Các chai đựng khí được cân bằng cân điện tử. Kết quả cân được ghi trong hàng thứ 2 bảng dưới.
Sách bài tập Vật Lí 12 Bài 11: Phương trình trạng thái của khí lí tưởng - Kết nối tri thức
Câu 11.9 trang 34 Sách bài tập Vật Lí 12: Có ba chai thuỷ tinh giống nhau (khối lượng và dung tích bằng nhau) đựng các chất khí khác nhau (He, C4H10, CO2) ở cùng nhiệt độ 20 °C và áp suất 1,913.105 Pa. Các chai đựng khí được cân bằng cân điện tử. Kết quả cân được ghi trong hàng thứ 2 bảng dưới.
1. Tính các giá trị còn trống trong bảng, biết khối lượng của chai khi chưa chứa khí là 378,68 g
2. So sánh các số liệu tìm được trong hàng cuối. Có phải chúng ta có thể dự đoán được kết quả so sánh này không? Tại sao?
3. Hãy dùng phương trình trạng thái của khí lí tưởng để tìm lại các giá trị của n trong bảng.
|
Khí |
He |
C4H10 |
CO2 |
|
Kết quả cân (g) |
378,86 |
381,34 |
380,70 |
|
Khối lượng khí m (g) |
|
|
|
|
Khối lượng mol M (g/mol) |
|
|
|
|
Số mol n |
|
|
|
Lời giải:
1.
|
Khí |
He |
C4H10 |
CO2 |
|
Kết quả cân (g) |
378,86 |
381,34 |
380,70 |
|
Khối lượng khí m (g) |
0,18 |
2,66 |
2,02 |
|
Khối lượng mol M (g/mol) |
4 |
58 |
44 |
|
Số mol n |
0,045 |
0,045 |
0,045 |
2. Số mol trong các chai bằng nhau. Có thể tiên đoán được dựa trên phương trình: pV = nRT
3. Hướng dẫn cách làm. Ví dụ với chai chứa CO2.
- Dựa vào thể tích của 1 mol khí CO2 ở điều kiện chuẩn để xác định thể tích của một mol khí CO2 ở điều kiện (T = 293 K và p = 1,913.105 Pa), từ đó suy ra thể tích của 2,02 g khí CO2 ở điều kiện (T = 293 K và p = 1,913.105 Pa).
- Áp dụng phương trình pV = nRT cho khí CO2 với các dữ liệu (V = 0,58 lít = 0,58.10-3 m3); T = 293 K; p = 1,913.105 Pa và R = 8,31 để tính n.
Lời giải SBT Vật Lí 12 Bài 11: Phương trình trạng thái của khí lí tưởng hay khác: