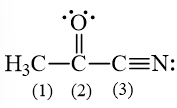Giải Chuyên đề Hóa học 10 Kết nối tri thức trang 12
Haylamdo biên soạn và sưu tầm lời Giải Chuyên đề Hóa học 10 trang 12 trong Bài 1: Liên kết hóa học sách Kết nối tri thức. Với lời giải hay nhất, chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập Chuyên đề Hóa 10.
Chuyên đề Hóa học 10 trang 12 Kết nối tri thức
Câu hỏi 10 trang 12 Chuyên đề Hóa học 10: Các nguyên tử carbon (1), (2), (3) trong hình bên ở những trạng thái lai hóa nào?
Lời giải:
C (1) lai hóa sp3 bởi vì C này chỉ tạo liên kết đơn.
C (2) lai hóa sp2 bởi vì C này có tạo liên kết đôi.
C (3) lai hóa sp bởi vì C này có tạo liên kết ba.
Câu hỏi 11 trang 12 Chuyên đề Hóa học 10: Mô tả sự tạo thành các phân tử sau theo khái niệm lai hóa orbital.
a) Phân tử BeH2.
b) Phân tử SO2.
c) Phân tử NH3.
Lời giải:
a) Phân tử BeH2.
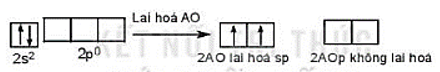
Cấu hình electron hóa trị của Be: 2s2.
Trong nguyên tử Be, một AO 2s tổ hợp với 1 AO 2p, tạo ra hai AO lai hóa sp.
Hai AO lai hóa sp của nguyên tử Be xen phủ với hai AO s của hai nguyên tử H tạo thành hai liên kết σ giữa Be – H.
b) Phân tử SO2.
Cấu hình electron hóa trị của S: 3s23p4.
Trong nguyên tử S, một AO 3s lai hóa với hai AO p, tạo ra ba AO lai hóa sp2.
S còn AO p chứa 1 electron độc thân sẽ xen phủ 1 AO p chứa 1 electron độc thân của O hình thành liên kết π và AO chưa lai hóa có 1 electron độc thân sẽ tiếp tục xen phủ với OA p của nguyên tử O đó để hình thành liên kết σ. Với nguyên tử O còn lại thì nguyên tử S dùng AO chứa 2 electron để xen phủ với 2 AO chứa electron độc thân của nguyên tử O còn lại.
c) Phân tử NH3.
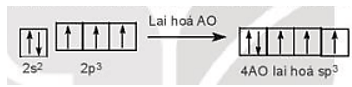
Cấu hình electron hóa trị của N: 2s22p3.
Trong nguyên tử N, 1 AO 2s và 3 AO 2p của nguyên tử N lai hóa với nhau tạo nên 4 AO lai hóa sp3 giống hệt nhau, hướng về 4 đỉnh của hình tứ diện đều. Trên 3 AO lai hóa có electron độc thân. Trên AO lai hóa còn lại có cặp electron ghép đôi.
Ba AO lai hóa chứa electron độc thân của nguyên tử N xen phủ với 3 AO 1s chứa electron độc thân của 3 nguyên tử H, tạo nên 3 liên kết σ.
Câu hỏi 12 trang 12 Chuyên đề Hóa học 10: Cho các phân tử NCl3, SO3, CO2.
a) Nguyên tử trung tâm trong các phân tử trên ở trạng thái lai hóa nào?
b) Phân tử nào không phân cực, phân tử nào phân cực? Vì sao?
Lời giải:
a) Trong phân tử NCl3, nguyên tử N là nguyên tử trung tâm lai hóa sp3.
Trong phân tử SO3, nguyên tử S là nguyên tử trung tâm, lai hóa sp2.
Trong phân tử CO2, nguyên tử C là nguyên tử trung tâm, lai hóa sp.
b) Phân tử NCl3, SO3 phân cực vì liên kết giữa nguyên tử trung tâm với nguyên tử còn lại là liên kết phân cực.
Phân tử CO2 không phân cực vì hai liên kết phân cực C = O bị triệt tiêu do phân tử có dạng đường thẳng.
Em có thể trang 12 Chuyên đề Hóa học 10: Vận dụng công thức phân tử theo mô hình VSEPR đề dự đoán dạng hình học và vận dụng khái niệm lai hoá orbital để giải thích dạng hình học đã dự đoán theo công thức phân tử theo mô hình VSEPR.
Lời giải:
Mô hình VSEPR được sử dụng để mô tả dạng hình học của các phân tử dựa trên lực đẩy giữa các cặp electron hóa trị. Để sử dụng mô hình VSEPR, công thức phân tử của chất được viết dưới dạng AXnEm. Trong đó:
A: nguyên tử trung tâm;
X: nguyên tử liên kết với nguyên tử A; n là số nguyên tử;
E: cặp electron hóa trị chưa liên kết của nguyên tử A; m là số cặp electron;
Lưu ý: Nếu nguyên tử trung tâm lẻ một electron thì electron đó vẫn được tính tương đương một cặp electron.
+ Trường hợp AXn (với n = 2, 3, 4, …)
• Với n = 2, phân tử có cấu trúc thẳng.
• Với n = 3, phân tử có cấu trúc tam giác phẳng.
• Với n = 4, phân tử có cấu trúc tứ diện.
+ Trường hợp AXnEm
• Với dạng AX2E, phân tử có dạng góc.
• Với dạng AX3E, phân tử có dạng tháp tam giác.
• Với dạng AX2E2, phân tử có dạng góc.
Có một số trường hợp mô hình VSEPR không giải thích được hình dạng phân tử nhưng có thể giải thích theo sự lai hóa orbital nguyên tử như CH4, NF3, …
Có 3 trạng thái lai hóa cơ bản: lai hóa sp3, lai hóa sp2 và lai hóa sp.
Lời giải bài tập Chuyên đề học tập Hóa học 10 Bài 1: Liên kết hóa học Kết nối tri thức hay khác: