Giải Chuyên đề Hóa học 10 trang 6 Cánh diều
Haylamdo biên soạn và sưu tầm lời Giải Chuyên đề Hóa học 10 trang 6 trong Bài 1: Liên kết hóa học và hình học phân tử sách Cánh diều. Với lời giải hay nhất, chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập Chuyên đề Hóa 10.
Chuyên đề Hóa học 10 trang 6 Cánh diều
Mở đầu trang 6 Chuyên đề học tập Hóa học 10: Theo em, dạng hình học nào sau đây của hai phân tử carbon dioxide và nước là đúng?
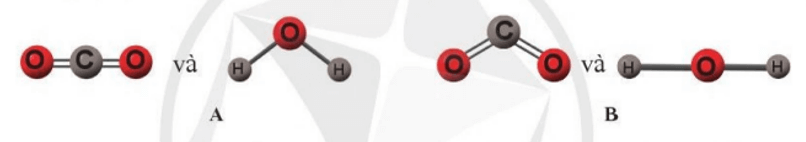
Lời giải:
Đáp án A
Đối với phân tử CO2
Công thức Lewis của CO2 là
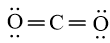
Nguyên tử trung tâm C có 2 liên kết (đôi) xung quanh tương ứng với 2 đám mây electron hóa trị. Công thức VSEPR của CO2 là AE2
Do 2 đám mây electron (liên kết đôi nối với O) phân bố thẳng hàng với nguyên tử C nên phân tử CO2 có dạng thẳng.
Đối với phân tử H2O
Công thức Lewis của H2O là
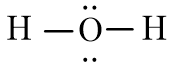
Xung quanh nguyên tử trung tâm O có 4 đám mây E (hai cặp electron chưa liên kết và hai cặp electron chung). Chiếm 4 khu vực điện tích âm đẩy nhau để góc hóa trị lớn nhất là 109,5o.
Tuy nhiên, do cặp electron chưa liên kết chiếm khoảng không gian lớn hơn so với các cặp electron liên kết, tương tác đẩy giữa các cặp electron chưa liên kết lớn hơn tương tác đẩy giữa các cặp electron liên kết, nên góc liên kết thực tế bằng 104,5o, nhỏ hơn góc hóa trị theo lí thuyết (109,5o). Phân tử có dạng góc.
Câu hỏi 1 trang 6 Chuyên đề học tập Hóa học 10: Những electron như thế nào được gọi là:
a) Electron hóa trị
b) Electron chung
c) Electron hóa trị riêng
Lời giải:
a) Electron hóa trị là những electron ở các orbital của lớp ngoài cùng và phân lớp sát ngoài cùng chưa bão hòa, có thể tham gia vào việc hình thành liên kết hóa học.
b) Electron chung là những electron hóa trị mà tham gia vào việc hình thành liên kết hóa học.
c) Electron hóa trị riêng là những electron hóa trị nhưng không tham gia vào việc hình thành liên kết hóa học.
Ví dụ:
- Nguyên tử Cl có có cấu hình electron là 1s22s22p63s23p5
⇒ Nguyên tử Cl có 7 electron hóa trị
- Phân tử Cl2 có liên kết giữa hai nguyên tử Cl được thực hiện nhờ 1 đôi electron góp chung; các electron còn lại được gọi là electron hóa trị riêng.
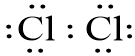
Câu hỏi 2 trang 6 Chuyên đề học tập Hóa học 10: Viết công thức cấu tạo của CO2 và H2O
Lời giải:
Lời giải bài tập Chuyên đề học tập Hóa học 10 Bài 1: Liên kết hóa học và hình học phân tử Cánh diều hay khác:

