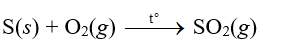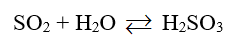Giải Chuyên đề Hóa học 10 Chân trời sáng tạo trang 62
Haylamdo biên soạn và sưu tầm lời Giải Chuyên đề Hóa học 10 trang 62 trong Bài 9: Thực hành thí nghiệm hóa học ảo sách Chân trời sáng tạo. Với lời giải hay và chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập Chuyên đề Hóa 10.
Chuyên đề Hóa học 10 trang 62 Chân trời sáng tạo
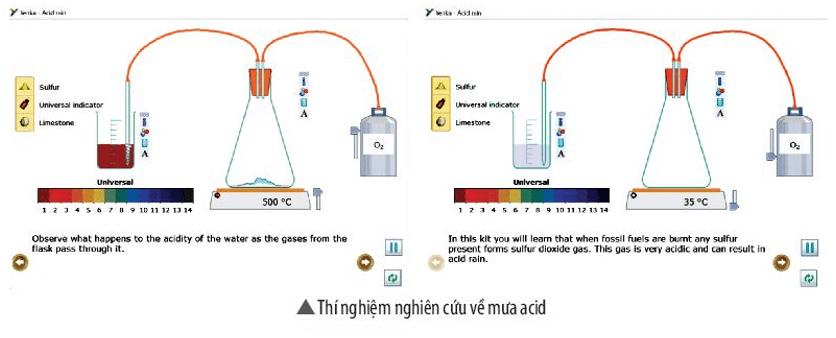
Bài 1 trang 62 Chuyên đề Hóa học 10: Sử dụng cửa sổ Open – local của phần mềm Yenka nghiên cứu về mưa acid (theo hình hướng dẫn sau). Rút ra kết luận từ kết quả thí nghiệm.
Lời giải:
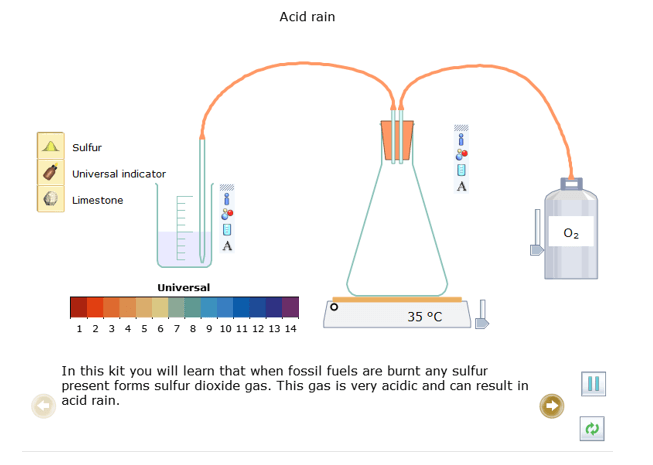
Bước 1: Nhấp chuột vào thể Open – local, chọn Acids, Bases and Salts → Acid rain, mô phỏng đã được thiết kế xuất hiện ở màn hình.
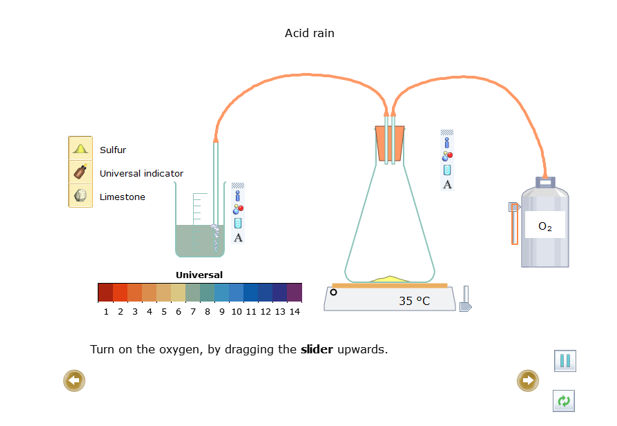
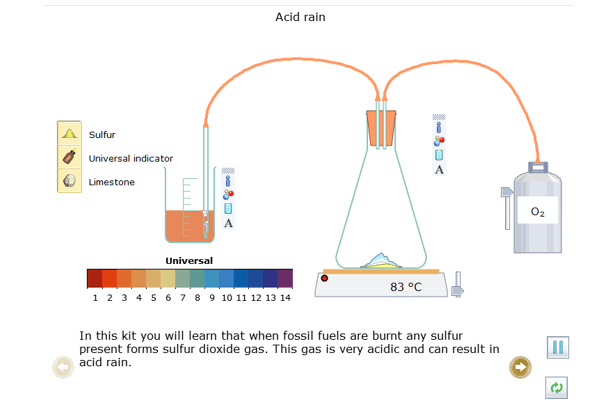
Trong thí nghiệm này em sẽ được hiểu rằng khi nhiên liệu hóa thạch bị đốt cháy thì sulfur (lưu huỳnh) sẽ chuyển thành khí sulfur dioxide (SO2). Khí này có tính acid rất cao và có thể dẫn đến mưa acid.
Bước 2: Nhấp chuột vào Next page 
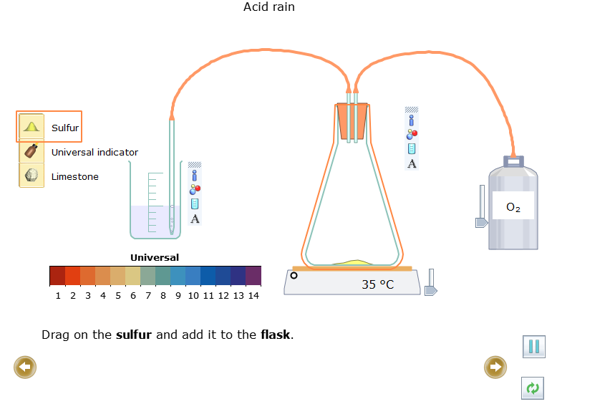
- Kéo Sulfur 
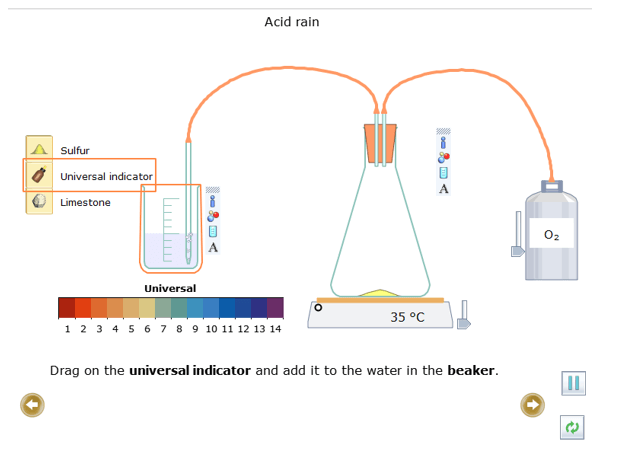
- Kéo 
- Bật bình khí oxygen bằng cách kéo thanh trượt lên trên
- Kéo tay cầm của thanh trượt trên bếp điện lên trên, cho đến khi sulfur bắt đầu đốt cháy.
- Quan sát điều gì xảy ra với tính acid của nước khi các khí từ bình đi qua nó.
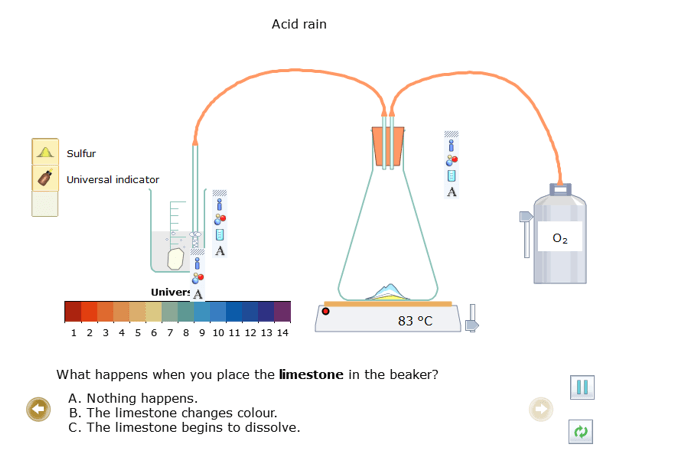
- Kéo đá vôi 
Bước 3: Ghi lại kết quả thí nghiệm và nhận xét
- Kết quả thí nghiệm:
+ Sulfur cháy trong oxygen với ngọn lửa màu xanh sáng.
+ Có khí thoát ra được dẫn vào cốc nước.
+ Khí này làm dung dịch trong cốc chuyển thành màu đỏ nhạt
+ Cho đá vôi vào dung dịch trong cốc thấy đá vôi tan, dung dịch từ màu đỏ chuyển thành không màu. Có khí thoát ra từ cốc.
- Nhận xét:
+ Sulfur cháy trong oxygen mãnh liệt với ngọn lửa màu xanh sáng tạo khí sulfur dioxide. Phương trình hóa học:
+ Khí SO2 tan trong nước tạo dung dịch làm chỉ thị chuyển thành màu đỏ nhạt. Do có SO2 phản ứng với nước tạo H2SO3. H2SO3 có tính acid.
+ Cho đá vôi vào cốc có khí thoát ra từ cốc do có phản ứng:
CaCO3 + H2SO3 → CaSO3↓ + H2O + CO2↑
Acid phản ứng hết tạo môi trường trung tính.
Bài 2 trang 62 Chuyên đề Hóa học 10: Sử dụng thể Open – local của phần mềm Yenka, thực hiện thí nghiệm ảnh hưởng của nhiệt độ lên tốc độ phản ứng “Temperature and rate”. Phân tích và lí giải kết quả của thí nghiệm.
Lời giải:
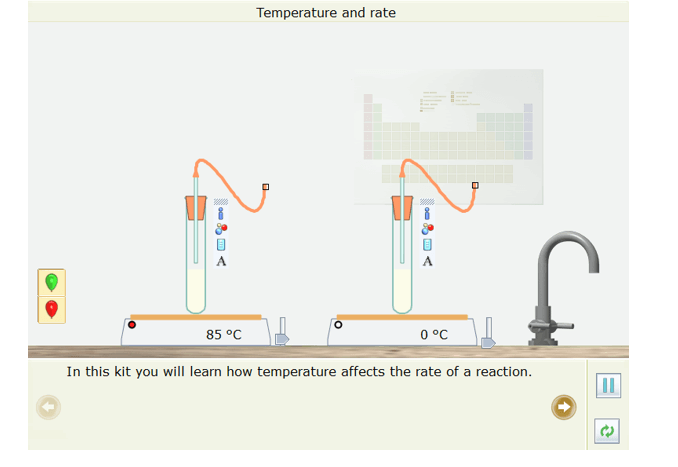
Bước 1: Nhấp chuột vào thể Open – local, chọn Reaction → Temperature and rate. Mô phỏng đã được thiết kế xuất hiện ở màn hình
Bước 2: Nhấp chuột vào Next page 
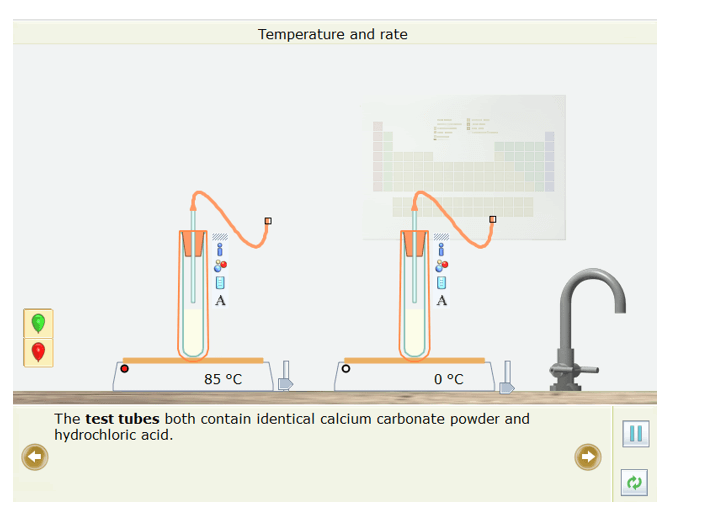
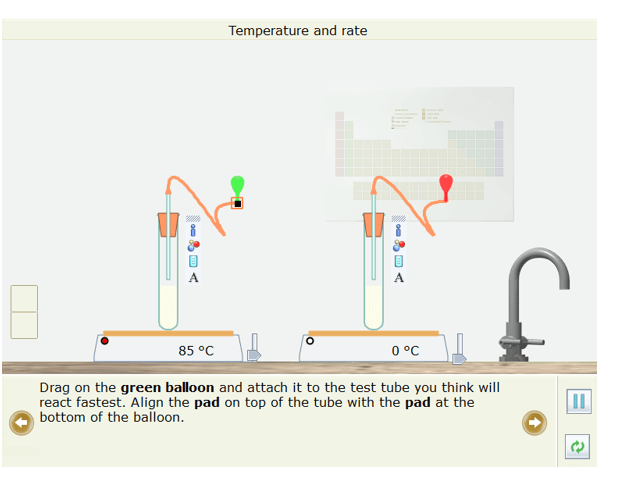
- Cả hai ống nghiệm đều chứa bột calcium carbonate và hydrochloric giống hệt nhau
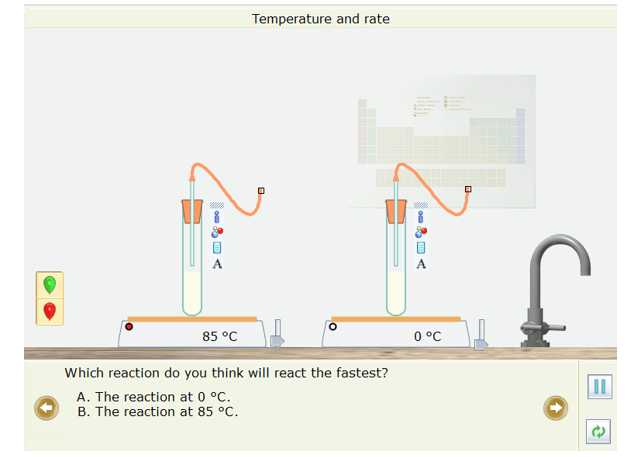
- Em hãy dự đoán xem phản ứng ở ống nghiệm nào nhanh nhất?
- Kéo quả bóng bay màu xanh lá cây lên và gắn nó vào ống nghiệm em cho là sẽ phản ứng nhanh nhất. Căn chỉnh miếng đệm trên đầu ống với miếng đệm ở đáy của quả bóng bay. Tương tự gắn quả bóng màu đỏ vào ống nghiệm mà em cho rằng sẽ phản ứng chậm nhất.
- Nhấp chuột vào nút Play/Pause 
Bước 3: Ghi lại kết quả thí nghiệm và nhận xét
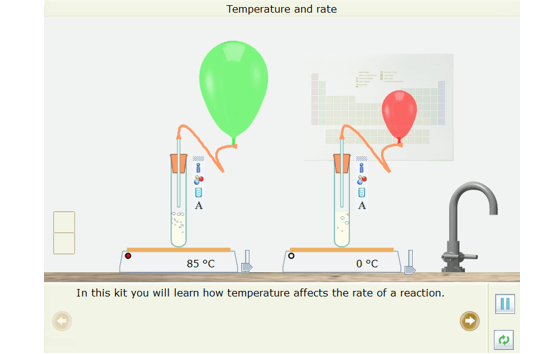
- Kết quả: Quả bóng ở ống nghiệm được đun nóng đến 85oC to lên nhanh hơn và vỡ trước.
- Nhận xét: Phương trình hóa học của phản ứng:
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + CO2(g) + H2O(l)
Quả bóng ở ống nghiệm được đun nóng đến 85oC to lên nhanh hơn. Chứng tỏ nhiệt độ càng cao thì tốc độ phản ứng càng lớn.
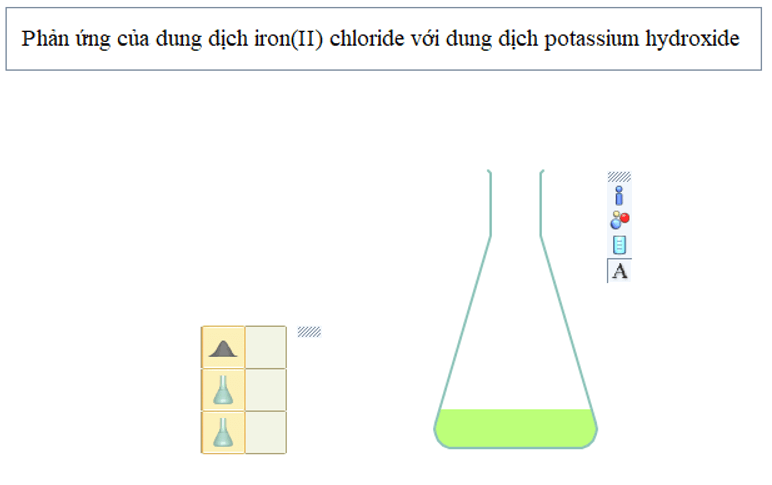
Bài 3 trang 62 Chuyên đề Hóa học 10: Hãy thiết kế thí nghiệm (thẻ New): Phản ứng của dung dịch iron(II) chloride 1M (FeCl2) với dung dịch potassium hydroxide 1 M (KOH).
a) Ghi rõ các bước chuẩn bị hóa chất, dụng cụ, cách tiến hành thí nghiệm.
b) Nêu hiện tượng xảy ra và giải thích.
Lời giải:
Bước 1: Nhấp chuột vào thẻ New, chọn Presentation 
Bước 2: Lấy hóa chất
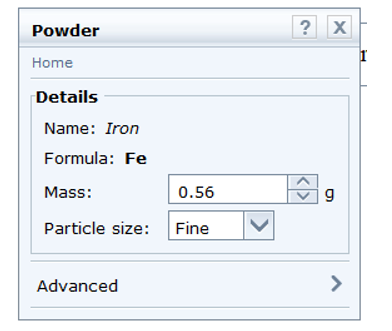
- Chọn Fe: Nhấp chuột vào thẻ Chemicals → Metal → Iron. Kéo thả vào khay.
Nhấp vào thông số khối lượng, điều chỉnh khối lượng Fe về 0,56 gam.
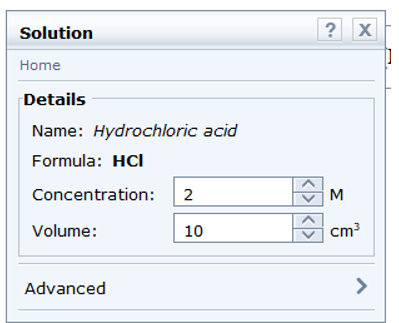
- Chọn hydrochloric acid: Chemicals → Acids → hydrochloric acid. Kéo thả vào khay. Nhấp vào các thông số về nồng độ và thể tích để điều chỉnh cho phù hợp với thí nghiệm. Chọn nồng độ 2 M và thể tích 10 cm3
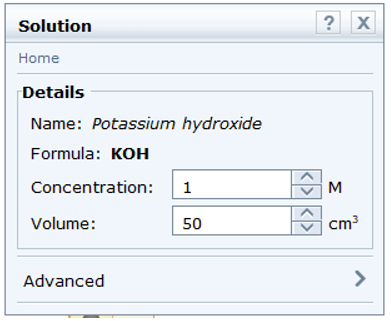
- Chọn dung dịch potassium hydroxide: Chemicals → Alkalis → Potassium hydroxide. Thông số về nồng độ là 1M phù hợp với thí nghiệm nên không cần điều chỉnh.
Bước 3: Lấy dụng cụ
- Chọn bình tam giác: Nhấp chuột vào thẻ Glassware → Standard → Erlenmeyer flask
Bước 4: Nhấp nút Play/Pause 
Nhấn nút Play/Pause trên thanh công cụ để thí nghiệm bắt đầu diễn ra, quan sát hiện tượng xảy ra. Muốn phản ứng xảy ra nhanh hay chậm, nhấp chuột vào nút Simulation Speed
Nhấp nút Play/Pause 
Nhấn nút Play/Pause trên thanh công cụ để thí nghiệm bắt đầu diễn ra, quan sát hiện tượng xảy ra. Muốn phản ứng xảy ra nhanh hay chậm, nhấp chuột vào nút Simulation Speed
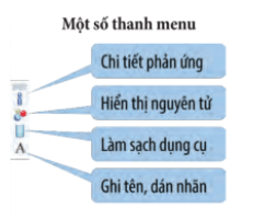
Bước 5: Sau khi các chất phản ứng với nhau, nhấn chuột vào các icon bên phải của dụng cụ để biết các thông tin:
Bước 6: Quan sát – Giải thích thí nghiệm
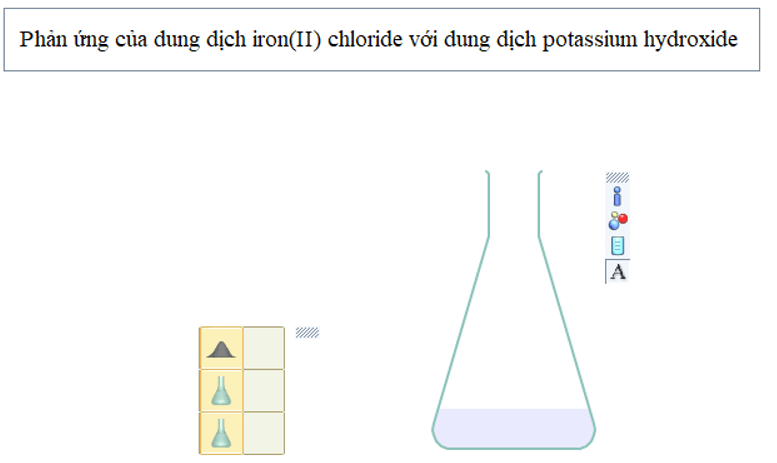
Hiện tượng:
- Đầu tiên iron (Fe) tan trong HCl để được dung dịch màu xanh, có khí thoát ra (coi thể tích dung dịch thay đổi không đáng kể sau phản ứng);
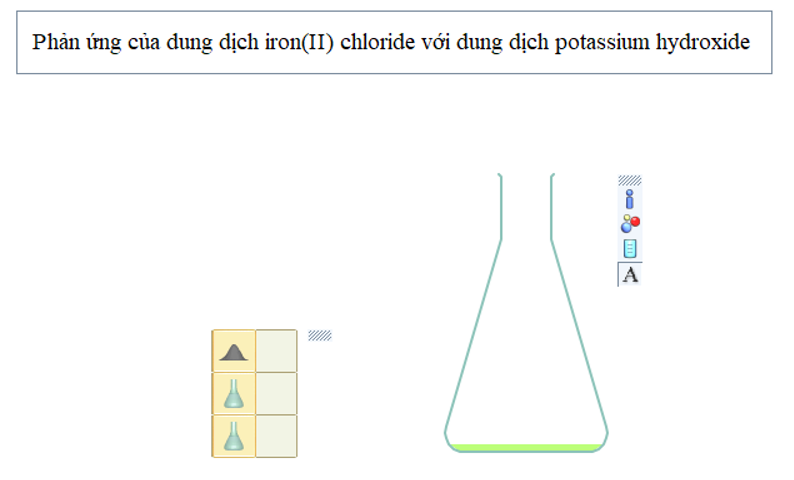
- Thêm tiếp dung dịch potassium hydroxide vào bình phản ứng thu được kết tủa màu trắng hơi xanh;
Giải thích bằng phương trình hóa học:
Fe + 2HCl → FeCl2 + H2↑
FeCl2 + 2KOH → Fe(OH)2↓ + 2KCl
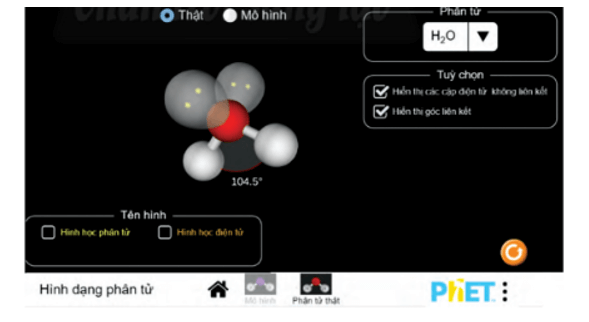
Bài 4 trang 62 Chuyên đề Hóa học 10: Thực hành thí nghiệm “Hình dạng phân tử” bằng phần mềm PhET. Rút ra kết luận từ kết quả thu được.
Lời giải:
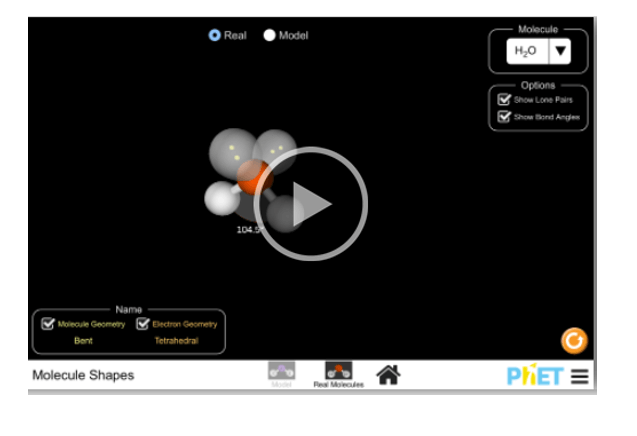
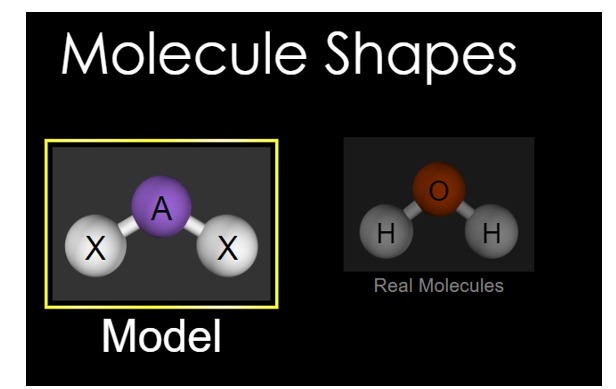
Bước 1: Bấm vào hình tam giác sẽ xuất hiện dạng mô hình (Model) và dạng phân tử thật (Real Molecules). Chọn dạng phân tử thật (Real Molecules)
Bước 2: Sau đó hiện màn hình hiển thị mô hình phân tử.
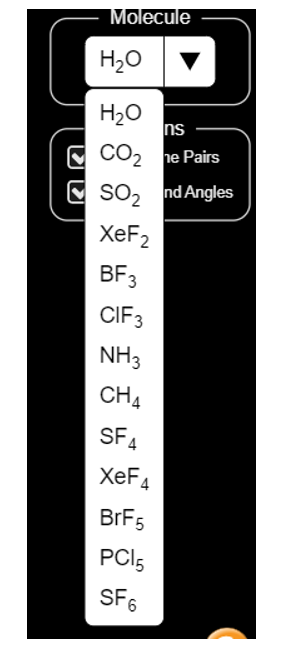
Chọn phân tử cần quan sát ở mục Molecule
- Tích chuột vào Show Lone Pairs sẽ hiển thị các cặp electron riêng.
Tích chuột vào Show Bond Angles sẽ hiển thị góc liên kết.
Nhấn giữ chuột vào phân tử để xoay theo ý muốn.
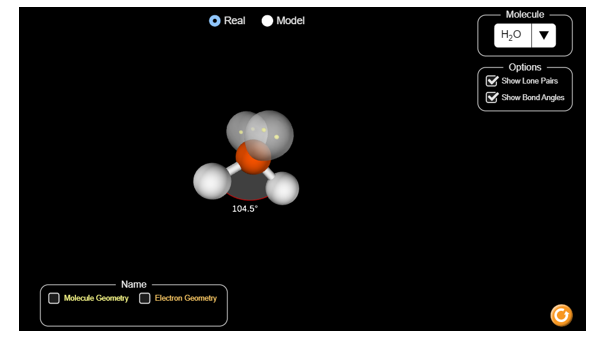
Bước 3: Quan sát, rút ra nhận xét, kết luận.
Xung quanh nguyên tử trung tâm O có hai cặp electron chưa liên kết và hai cặp electron chung với nguyên tử H. Chiếm 4 khu vực điện tích âm đẩy nhau để góc hóa trị lớn nhất là 109,5o.
Tuy nhiên, do cặp electron chưa liên kết chiếm khoảng không gian lớn hơn so với các cặp electron liên kết, tương tác đẩy giữa các cặp electron chưa liên kết lớn hơn tương tác đẩy giữa các cặp electron liên kết, nên góc liên kết 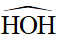
Phân tử có dạng góc.