Tính nồng độ H+ (mol/l) trong các dung dịch sau
Bài 6: Phản ứng trao đổi ion trong dung dịch các chất điện li
Bài 11 (trang 29 sgk Hóa 11 nâng cao): Tính nồng độ H+ (mol/l) trong các dung dịch sau:
a) CH3COONa 0,10M (Kb của CH3COO- là 5,71.10-10);
b) NH4Cl 0,10M (Ka của NH4+ là 5,56.10-10).
Lời giải:
a)
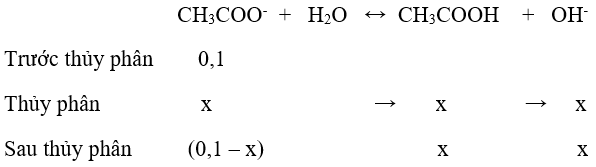
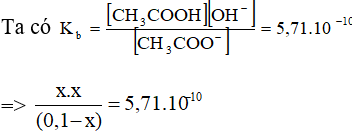
Vì x << 0,1 ⇒ (0,1 – x) ≈ 0,1
⇒ x.x = 0,1.5,71.10-10 = 0,571.10-10
⇒ x = 0,76.10-5.
⇒ [OH-] = 0,76.10-5 mol/lít
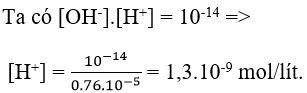
b)
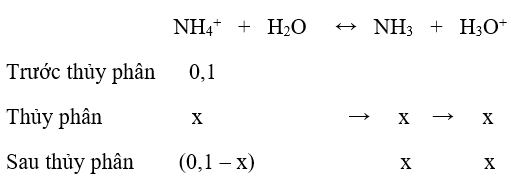
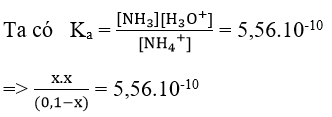
Vì x << 0,1 ⇒ (0,1 – x) ≈ 0,1
⇒ x.x = 0,1.5,56.10-10 = 0,556.10-10
⇒ x = 0,75.10-5.
⇒ [H3O+] = 0,75.10-5 mol/lít.

