Giải Hóa 12 nâng cao Bài 54: Bài thực hành 8: Nhận biết một số ion trong dung dịch
Giải Hóa 12 nâng cao Bài 54: Bài thực hành 8: Nhận biết một số ion trong dung dịch
Haylamdo biên soạn và sưu tầm lời giải bài tập Hóa học 12 Bài 54: Bài thực hành 8: Nhận biết một số ion trong dung dịch hay, chi tiết bám sát sách Hóa học lớp 12 nâng cao giúp bạn biết cách làm bài tập Hóa 12.

Thí nghiệm 1. Nhận biết NH4+ và CO32-
- Tiến hành TN:
+ Ống 1: Lấy dd (NH4)2CO3 cho tác dụng với dd HCl loãng, quan sát hiện tượng
+ Lần lượt cho dd (NH4)2CO3 (ống 2) và Na2CO3 (ống 3) tác dụng với lượng dư dd NaOH, đun nóng nhẹ, để trên miệng mỗi ống nghiệm 1 mảnh giấy quỳ tím ẩm.
- Hiện tượng:
+ Ống 1: Có khí không màu thoát ra
+ Ống 2: Có khí mùi khai thoát ra
+ Ống 3: Không có hiện tượng gì
- Giải thích, PTHH:
+ Ống 1: Tạo khí do xảy ra phản ứng trao đổi giữa muối (NH4)2CO3 và axit HCl
(NH4)2CO3 + 2HCl → 2NH4Cl + CO2 + H2O
+ Ống 2: Có khí mùi khai do (NH4)2CO3 tác dụng với NaOH sinh ra NH4OH
Đun nóng nhẹ phân hủy ngay thành khí NH3 có mùi khai
(NH4)2CO3 + 2NaOH → 2NH4OH + Na2CO3
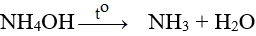
+ Ống 3: Muối Na2CO3 không phản ứng với NaOH
Thí nghiệm 2. Nhận biết các ion Fe2+, Fe3+
- Tiến hành TN:
+ Cho dd KSCN tác dụng với dd Fe3+. Quan sát
+ Cho dd KOH (hoặc NH3) tác dụng với dd Fe3+. Để lắng kết tủa
+ Cho dd Fe2+ tác dụng với dd NaOH (hoặc NH3). Để lắng kết tủa
- Hiện tượng, PTHH:
+ Cho dd KSCN tác dụng với dd Fe3+ tạo phức màu đỏ máu
Fe3+ + 3SCN- → Fe(SCN)3
+ Cho dd KOH tác dụng với dd Fe3+ tạo kết tủa nâu đỏ
Fe3+ + 3OH- → Fe(OH)3
+ Cho dd Fe2+ tác dụng với dd NaOH tạo kết tủa trắng xanh
Fe2+ + 2OH- → Fe(OH)2
Để 1 thời gian kết tủa chuyển màu vàng nâu do:
2Fe(OH)2 + 1/2 O2 + H2O → 2Fe(OH)3
Thí nghiệm 3. Nhận biết cation Cu2+
- Tiến hành TN:
+ Lấy vào ống nghiệm 1 ít dd Cu2+
+ Thêm từ từ dd NH3 loãng
+ Tiếp tục thêm NH3 đến khi tủa tan hết.
- Hiện tượng: Tạo kết tủa xanh, sau đó kết tủa tan tạo phức có màu xanh lam đặc trưng.
- Giải thích: Lúc đầu Cu2+ tác dụng với NH3 tạo kết tủa Cu(OH)2.
Sau đó kết tủa tan trong NH3 dư tạo phức.
PTHH:
Cu2+ + 2NH3 + 2H2O → Cu(OH)2 + 2NH4+
Cu(OH)2 + 4NH3 → [Cu(NH3)4]2+ + 2OH-
Thí nghiệm 4. Nhận biết anion NO3-
- Tiến hành TN:
+ Lấy vào ống nghiệm 1 ít dd KNO3, thêm vào 1 ít bột Cu, đun nóng nhẹ.
+ Thêm vài giọt dd H2SO4 loãng, đun nhẹ.
- Hiện tượng: Cu tan tạo dung dịch màu xanh, xuất hiện khí không màu bị hóa nâu ngoài không khí.
- Giải thích: Bột Cu tan tạo thành dung dịch màu xanh, tạo khí NO bay lên tác dụng với oxi trong không khí tạo thành khí NO2 màu đỏ nâu.
PTHH:
3Cu + 8H+ + 2NO3- → 3Cu2+ + 2NO + 4H2O
2NO + O2 → 2NO2

