Đốt cháy hoàn toàn 2,04 gam hợp chất A, thu được 1,08 g H2O Bài 9 trang 139 Hóa 10
Bài 32: Hiđro sunfua - Lưu huỳnh đioxit - Lưu huỳnh trioxit
Bài 9 trang 139 Hóa 10: Đốt cháy hoàn toàn 2,04 gam hợp chất A, thu được 1,08 g H2O và 1,344 l SO2 (đktc).
a) Hãy xác định công thức phân tử của hợp chất A.
b) Dẫn toàn bộ lượng hợp chất A nói trên qua dung dịch axit sunfuric đặc thấy có kết tủa màu vàng xuất hiện :
- Hãy giải thích hiện tượng và viết các phương trình phản ứng xảy ra.
- Tính khối lượng kết tủa thu được.
Trả lời
a) Xác định công thức phân tử của hợp chất A.
nSO2 = 1,344/22,4 = 0,06 mol → mS = 1,92 gam
nH2O = 1,08/18 = 0,06 mol → mH = 0,12 gam.
Như vậy hợp chất A chỉ gồm hai nguyên tố H và S.
Đặt công thức của hợp chất A là HxSy.
Ta có tỉ lệ x : y = 0,06 : 0,12 = 1 : 2.
Vậy công thức phân tử của A là H2S.
b) Phương trình hóa học của phản ứng:
nH2S = 2,04/34 = 0,06 mol
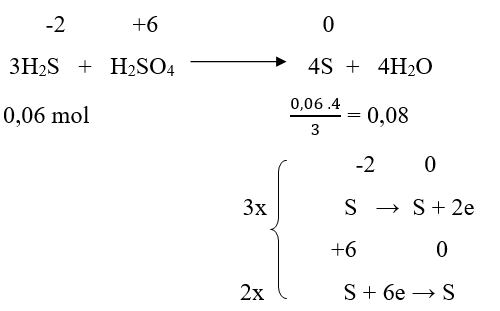
mS = 0,08.32 = 2,56g

