Bài 29.8, 29.9, 29.10 trang 38 SBT Hóa học 9
Bài 29.8, 29.9, 29.10 trang 38 SBT Hóa học 9
Bài 29.8 trang 38 Sách bài tập Hóa học 9: Nung 150 kg CaCO3 thu được 67,2 kg CaO. Hiệu suất của phản ứng là
A. 60% ; B. 40% ; C. 80% ; D. 50%.
Lời giải:
Đáp án C.
CaCO3 to CaO + CO2
mCaO = 56/100.x.150 = 84 (kg)
H% = 67,2/84 x 100% = 80%
Bài 29.9 trang 38 Sách bài tập Hóa học 9: Nung nóng m gam hỗn hợp CaCO3 và MgCO3 đến phản ứng hoàn toàn, sau phản ứng thu được 2,72 gam hỗn hợp 2 oxit và 1344 ml khí CO2 (ở đktc). Hãy tính giá trị của m.
Lời giải:
Phương trình hóa học của phản ứng:
CaCO3 to CaO + CO2
MgCO3 to MgO + CO2
nCaCO3 = x; nMgCO3 = y
nCO2 = 1344/22400 = 0,06
Ta có hệ phương trình
56x + 40y = 2,72
x + y = 0,06
Giải ra, ta có: x = 0,O2(mol); y = 0,04(mol)
m = mCaCO3 + mMgCO3 = 0,O2 x 100 + 0,04 x 84 = 5,36g
Bài 29.10 trang 38 Sách bài tập Hóa học 9: Cho 1,06 gam muối cacbonat kim loại hoá trị I tác dụng hết với dung dịch HCl thấy thoát ra 224 mi khí cacbonic (ở đktc). Xác định công thức phân tử muối cacbonat.
Lời giải:
Gọi M là kí hiệu nguyên tử khối của kim loại hoá trị I. Công thức muối là M2CO3. Phương trình hoá học của phản ứng :
M2CO3 + 2HCl → 2MCl2 + H2O + CO2
(2M + 60)g 22400ml
1,06g 224ml
Theo phương trình hóa học trên ta có:
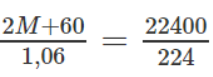
→ M = 23. Đó là muối Na2CO3

