Cho phương trình nhiệt hóa học sau:SO2 (g) + 1/2 O2 (g) SO3 (g) = − 98,5 kJLượng nhiệt giải phóng ra
Câu hỏi:
Cho phương trình nhiệt hóa học sau:
SO2 (g) +  O2 (g)
O2 (g) 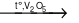 SO3 (g)
SO3 (g) 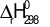 = − 98,5 kJ
= − 98,5 kJ
Lượng nhiệt giải phóng ra khi chuyển 76,8 gam SO2 (g) thành SO3 (g) là
A. 98,5 kJ;
B. 118,2 kJ;
C. 82,08 kJ;
D. 7564,8 kJ.
Trả lời:
Đáp án đúng là: B
SO2 (g) +  O2 (g)
O2 (g) 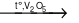 SO3 (g)
SO3 (g) 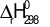 = − 98,5 kJ
= − 98,5 kJ
Theo phương trình nhiệt hóa học, ta có cứ chuyển 1 mol SO2 (g) thành SO3 (g) thì lượng nhiệt giải phóng là 98,5 kJ.
76,8 gam SO2 (g) có số mol là: 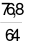 = 1,2 (mol)
= 1,2 (mol)
Vậy chuyển 76,8 gam SO2 (g) thành SO3 (g) thì lượng nhiệt giải phóng là:
98,5.1,2 = 118,2 (kJ)

 2H2O (g)
2H2O (g)