Giải SBT Hóa học 10 trang 16 Cánh diều
Haylamdo biên soạn và sưu tầm lời giải SBT Hóa học 10 trang 16 trong Bài 5: Lớp, phân lớp và cấu hình electron sách Cánh diều. Với lời giải chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập SBT Hóa học 10.
Giải SBT Hóa học 10 trang 16 Cánh diều
Bài 5.15 trang 16 sách bài tập Hóa học 10: Hãy cho biết những nguyên tử và ion (cation mang điện tích 1+, 2+ hoặc anion mang điện tích 1-, 2-) nào có cấu hình electron là 1s22s22p6.
Lời giải:
Số lượng electron trong cấu hình 1s22s22p6 là 10 electron.
- Nếu đây là cấu hình electron của nguyên tử thì nguyên tử phải có 10 electron, do đó Z = 10, đó là nguyên tử Ne.
- Nếu đây là cấu hình electron của cation Mn+ (n = 1, 2) thì cation này được tạo ra từ nguyên tử M bằng cách tách đi n electron:
M → Mn+ (10 electron) + ne
Vậy số electron trong nguyên tử M là: 10 + n.
+ Nếu n = 1, M có 11 electron nên Z = 11 ⇒ ion Na+ có cấu hình electron: 1s22s22p6.
+ Nếu n = 2, M có 12 electron nên Z = 12 ⇒ ion Mg2+ có cấu hình electron: 1s22s22p6.
- Nếu đây là ion Xn- (n = 1, 2) thì anion này được tạo ra từ X bằng cách nhận vào n electron.
Vậy số electron trong nguyên tử X là: 10 – n.
+ Nếu n = 1, X có 9 electron nên Z = 9 ⇒ ion F- có cấu hình electron: 1s22s22p6.
+ Nếu n = 2, X có 8 electron nên Z = 8 ⇒ ion O2- có cấu hình electron: 1s22s22p6.
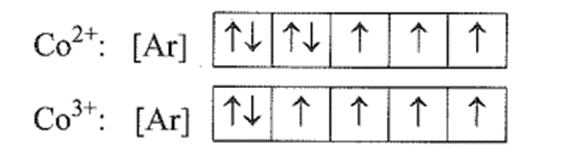
Bài 5.16 trang 16 sách bài tập Hóa học 10: Tại một khu vực của Úc, gia súc không phát triển mạnh mặc dù có thức ăn thô xanh thích hợp. Một cuộc điều tra cho thấy nguyên nhân là do không có đủ cobalt trong đất. Cobalt tạo thành cation ở hai dạng là Co2+ và Co3+ (Z = 27). Viết cấu hình electron của hai cation này và sơ đồ phân bố các electron vào các ô orbital. Cho biết số electron độc thân trong mỗi ion.
Lời giải:
Co có Z = 27 nên có cấu hình electron là: 1s22s22p63s23p63d74s2.
Khi Co mất đi 2 electron và 3 electron sẽ lần lượt tạo ra: Co2+ và Co3+. Các electron sẽ tách đi từ các lớp ngoài rồi tới lớp trong. Cấu hình electron của hai ion này là:
Co2+: 1s22s22p63s23p63d7
Co3+: 1s22s22p63s23p63d6
Sơ đồ phân bố electron vào các ô orbital:
Số electron độc thân trong Co2+ và Co3+ lần lượt là 3 và 4.
Bài 5.17 trang 16 sách bài tập Hóa học 10: Bromine (Z = 35) dễ phản ứng, trong khi krypton (Z = 36) tương đối trơ về mặt hóa học. Giải thích sự khác biệt này dựa trên cấu hình electron của chúng.
Lời giải:
- Cấu hình electron của bromine (Z = 35): [Ar]3d104s24p5.
Nguyên tử bromine có 7 electron ở lớp ngoài cùng là phi kim điển hình.
- Cấu hình electron của krypton (Z = 36): [Ar]3d104s24p6.
Nguyên tử krypton có 8 electron ở lớp ngoài cùng nên là khí hiếm.
Bài 5.18 trang 16 sách bài tập Hóa học 10: Cũng giống như nam châm, mỗi nguyên tử/ ion cũng có thể có từ tính (bị nam châm hút). Nếu nguyên tử/ ion có electron độc thân thì nó có từ tính và được gọi là chất thuận từ. Ngược lại, nguyên tử/ ion nếu không có electron độc thân thì được gọi là chất nghịch từ. Hãy giải thích vì sao nguyên tử Cu (Z = 29) thuận từ nhưng ion Cu+ lại nghịch từ.
Lời giải:
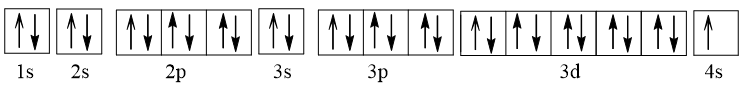
- Cấu hình electron của Cu (Z = 29): 1s22s22p63s23p63d104s1.
Viết gọn: [Ar]3d104s1.
Biểu diễn dưới dạng ô orbital nguyên tử:
Như vậy Cu có 1 electron độc thân nên thuận từ.
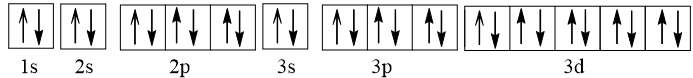
- Cu nhường đi 1 electron tạo thành ion Cu+ có cấu hình electron: 1s22s22p63s23p63d10.
Viết gọn: [Ar]3d10.
Biểu diễn dưới dạng ô orbital nguyên tử:
Như vậy Cu+ không có electron độc thân nên nghịch từ.
Lời giải sách bài tập Hóa học lớp 10 Bài 5: Lớp, phân lớp và cấu hình electron Cánh diều hay khác: