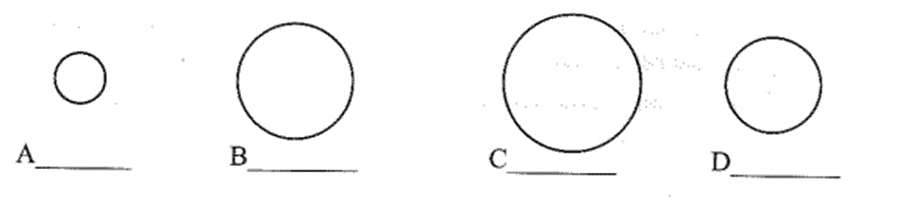Giải SBT Hóa học 10 trang 56 Cánh diều
Haylamdo biên soạn và sưu tầm lời giải SBT Hóa học 10 trang 56 trong Bài 17: Nguyên tố và đơn chất halogen sách Cánh diều. Với lời giải chi tiết hy vọng sẽ giúp các học sinh dễ dàng nắm được cách làm bài tập SBT Hóa học 10.
Giải SBT Hóa học 10 trang 56 Cánh diều
Bài 17.1 trang 56 sách bài tập Hóa học 10: Phát biểu nào sau đây không đúng khi nói về nguyên tử các nguyên tố nhóm VIIA?
A. Có 7 electron hóa trị.
B. Theo chiều tăng dần của điện tích hạt nhân nguyên tử thì độ âm điện giảm.
C. Theo chiều tăng dần điện tích hạt nhân nguyên tử thì khả năng hút cặp electron liên kết giảm.
D. Theo chiều tăng dần điện tích hạt nhân nguyên tử thì bán kính nguyên tử giảm.
Lời giải:
Đáp án đúng là: D
Phát biểu D không đúng vì: Trong nhóm VIIA, theo chiều tăng dần điện tích hạt nhân nguyên tử thì bán kính nguyên tử tăng.
Bài 17.2 trang 56 sách bài tập Hóa học 10:
a) Điền tên và kí hiệu các nguyên tố halogen bền vào vị trí các nguyên tố A, B, C, D bên dưới. Biết mỗi vòng tròn minh họa cho một nguyên tử với tỉ lệ kích thước tương ứng.
b) Viết công thức phân tử đơn chất của mỗi nguyên tố tương ứng.
c) Ở điều kiện nhiệt độ, áp suất thông thường, các đơn chất này tồn tại ở trạng thái nào? Từ đó, dự đoán thứ tự tăng nhiệt độ nóng chảy, nhiệt độ sôi tương ứng giữa chúng trong cùng điều kiện áp suất.
Lời giải:
a) Từ fluorine đến iodine bán kính nguyên tử tăng dần. Ta có kết quả điền như sau:
A: Fluorine, F;
B: Bromine, Br;
C: Iodine, I;
D: Chlorine, Cl.
b) Công thức phân tử đơn chất của mỗi nguyên tố tương ứng:
A: Fluorine, F2;
B: Bromine, Br2;
C: Iodine, I2;
D: Chlorine, Cl2.
c) Trạng thái các đơn chất ở điều kiện nhiệt độ, áp suất thông thường:
Đơn chất |
F2 |
Cl2 |
Br2 |
I2 |
Trạng thái |
Khí |
Khí |
Lỏng |
Rắn |
Từ trạng thái này dự đoán nhiệt độ nóng chảy, nhiệt độ sôi của các halogen tăng dần theo thứ tự: F2, Cl2, Br2, I2.
Bài 17.2 trang 56 sách bài tập Hóa học 10: Nguyên nhân dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine,
A. khối lượng phân tử và tương tác van der Waals đều tăng.
B. tính phi kim giảm và tương tác van der Waals tăng.
C. khối lượng phân tử tăng và tương tác van der Waals giảm.
D. độ âm điện và tương tác van der Waals đều giảm.
Lời giải:
Đáp án đúng là: A
Nguyên nhân dẫn đến nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen tăng từ fluorine đến iodine là do từ fluorine đến iodine, khối lượng phân tử và tương tác van der Waals đều tăng.
Lời giải sách bài tập Hóa học lớp 10 Bài 17: Nguyên tố và đơn chất halogen Cánh diều hay khác: