Bài 1.6, 1.7 trang 4 SBT Hóa học 9
Bài 1.6, 1.7 trang 4 SBT Hóa học 9
Bài 1.6 trang 4 Sách bài tập Hóa học 9: Cho 15,3 gam oxit của kim loại hoá trị II vào nước thu được 200 gam dung dịch bazơ với nồng độ 8,55%. Hãy xác định công thức của oxit trên.
Lời giải:
Cách 1: Đặt công thức hoá học của oxit là MO => công thức bazơ là M(OH)2
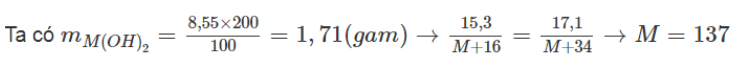
→ Công thức oxit là BaO.
Cách 2: mH2O(p/u) = mM(OH)2 - mMO = 17,1 - 15,3 = 1,8(g)
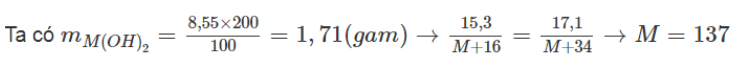
Công thức oxit là BaO
Bài 1.7 trang 4 Sách bài tập Hóa học 9: Cho 38,4 gam một oxit axit của phi kim X có hoá trị IV tác dụng vừa đủ với dung dịch NaOH thu được 400 gam dung dịch muối nồng độ 18,9%. Xác định công thức của oxit.
Lời giải:
Cách 1 : Đặt công thức của oxit là XO2.
mmuoi = 18x400/100 = 75,6 (g)
XO2 + 2NaOH → Na2XO3 + H2O
Theo phương trình hoá học
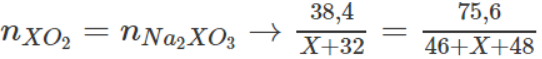
=> X = 32 => Công thức oxit là SO2.
Cách 2: mmuoi = 75,6(g) → mNa2O = 75,6 - 38,4 = 37,2(g)
nNa2O = 37,2/62 = 0,6 (mol)
nXO2 = nNa2O = 0,6 mol
→ MXO2 = 38,4/0,6 = 64(gam/mol)
→ X = 32
=> Công thức oxit là SO2.

