Giáo án Hóa học 12 Bài 21: Điều chế kim loại (tiết 2) mới nhất
Giáo án Hóa học 12 Bài 21: Điều chế kim loại (tiết 2) mới nhất
Haylamdo biên soạn và sưu tầm Với mục đích giúp các Thầy / Cô giảng dạy môn Hóa học dễ dàng biên soạn Giáo án Hóa học lớp 12, VietJack biên soạn Giáo án Hóa học 12 Bài 21: Điều chế kim loại (tiết 2) phương pháp mới theo hướng phát triển năng lực theo 5 bước bám sát mẫu Giáo án môn Hóa học chuẩn của Bộ Giáo dục. Hi vọng tài liệu Giáo án Hóa học 12 này sẽ được Thầy/Cô đón nhận và đóng góp những ý kiến quí báu.
A. CHUẨN KIẾN THỨC – KĨ NĂNG
I. KIẾN THỨC – KĨ NĂNG
1. Kiến thức
Hiểu được:
Nguyên tắc chung và các phương pháp điều chế kim loại (điện phân, nhiệt luyện, dùng kim loại mạnh khử ion kim loại yếu hơn).
2. Kĩ năng
- Lựa chọn được phương pháp điều chế kim loại cụ thể cho phù hợp.
- Quan sát thí nghiệm, hình ảnh, sơ đồ để rút ra nhận xét về phương pháp điều chế kim loại.
- Viết các phương trình hoá học điều chế kim loại cụ thể.
- Tính khối lượng nguyên liệu sản xuất được một lượng kim loại xác định theo hiệu suất hoặc ngược lại.
3. Thái độ: Hứng thú với môn học
4. Trọng tâm: Các phương pháp điều chế kim loại.
II. PHÁT TRIỂN NĂNG LỰC
* Năng lực:
1. Năng lực hợp tác
2. Năng lực phát hiện và giải quyết vấn đề
3. Năng lực giao tiếp
4. Năng lực sử dụng ngôn ngữ
5. Năng lực tư duy
* Phẩm chất: Yêu gia đình, quê hương đất nước; Nhân ái khoan dung; Trung thực, tự trọng, chí công, vô tư; Tự lập, tự tin, tự chủ; Có trách nhiệm với bản thân, cộng đồng, đất nước, nhân loại; Nghĩa vụ công dân.
B. CHUẨN BỊ
1. Giáo viên: mạt sắt, dung dịch đồng sunfat, cốc.
2. Học sinh: Ôn tập tính chất kim loại, học bài cũ
C. PHƯƠNG PHÁP VÀ KĨ THUẬT DẠY HỌC:
Phát vấn - Hoạt động nhóm - Trực quan
D. TIẾN TRÌNH BÀI DẠY
1. Hoạt động khởi động
1.1. Ổn định lớp: Kiểm tra sĩ số, đồng phục...
1.2. Kiểm tra bài cũ: Bỏ qua kiểm tra đầu giờ
2. Hoạt động hình thành kiến thức mới
Hoạt động của giáo viên |
Hoạt động của Học sinh – Phát triển năng lực |
Nội dung |
|
GV giao nhiệm vụ cho HS Nhóm 1, 3: Tìm hiểu điện phân hợp chất nóng chảy - Trình bày nguyên tắc, phạm vi áp dụng điện phân hợp chất nóng chảy - Viết PTHH của phản ứng xảy ra ở các điện cực và PTHH chung của sự điện phân khi điện phân nóng chảy Al2O3, MgCl2. Nhóm 2, 4: Tìm hiểu điện phân dung dịch - Trình bày nguyên tắc, phạm vi áp dụng điện phân dung dịch - Viết PTHH của phản ứng xảy ra ở các điện cực và PTHH chung của sự điện phân khi điện phân dung dịch CuCl2 GV yêu cầu các nhóm trình bày (do GV chỉ định), nhóm nào trình bày thì nhóm còn lại bổ sung, nhận xét GV chốt lại kiến thức Trong bình (bể) điện phân: Catot (-): xảy ra sự khử (quá trình thu e) Anot (+): xảy ra sự oxi hoá (qt nhường e). - GV giới thiệu với HS: các quá trình điện phân đang xét đều thực hiện với điện cực trơ. GV giới thiệu công thức Farađây dùng để tính lượng chất thu được ở các điện cực và giải thích các kí hiệu có trong công thức. GV nêu cho học sinh một số chú ý khi giải toán điện phân - Xác định đúng thứ tự nhường, nhận e ở các điện cực. - Xác định được thời điểm dừng điện phân. - Gv lấy ví dụ cụ thể để giải thích các đại lượng trong công thức. GV yêu cầu học sinh viết công thức tính ne (số mol e trao đổi) và số mol chất bị điện phân trong thời gian t. |
Hs thảo luận và trình bày Hs khác bổ sung, nhận xét Phát triển năng lực hợp tác, giao tiếp, năng lực sử dụng ngôn ngữ hóa học |
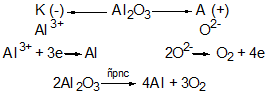
3. Phương pháp điện phân a) Điện phân hợp chất nóng chảy Nguyên tắc: Khử các ion kim loại bằng dòng điện bằng cách điện phân nóng chảy hợp chất của kim loại. Phạm vi áp dụng: Điều chế các kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al. Thí dụ 1: Điện phân Al2O3 nóng chảy để điều chế Al. Thí dụ 2: Điện phân MgCl2 nóng chảy để điều chế Mg. b) Điện phân dung dịch
Thí dụ: Điện phân dung dịch CuCl2 để điều chế kim loại Cu. c) Tính lượng chất thu được ở các điện cực Dựa vào công thức Farađây: m = m: Khối lượng chất thu được ở điện cực (g). A: Khối lượng mol nguyên tử của chất thu được ở điện cực. n: Số electron mà nguyên tử hoặc ion đã cho hoặc nhận I: Cường độ dòng điện (ampe). t: Thời gian điện phân (giây). |
..........................................
Tài liệu còn nhiều, mời bạn tải xuống để xem đầy đủ!

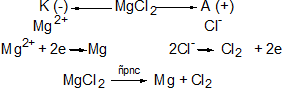
 Nguyên tắc: Điện phân dung dịch muối của kim loại.
Nguyên tắc: Điện phân dung dịch muối của kim loại.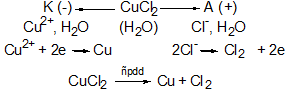
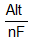 , trong đó:
, trong đó: