C3H8 + 5O2 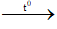 3CO2 + 4H2O - Cân bằng phương trình hoá học
3CO2 + 4H2O - Cân bằng phương trình hoá học
Phản ứng hoá học:
C3H8 + 5O2 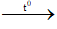
Điều kiện phản ứng
- Nhiệt độ
Cách thực hiện phản ứng
- Đốt cháy khí propan (C3H8) trong không khí thì thu được khí cacbonic và nước.
(Xét phản ứng xảy ra hoàn toàn và vừa đủ, không có chất dư)
Hiện tượng nhận biết phản ứng
- Dẫn sản phẩm cháy qua bình đựng nước vôi trong dư thấy có kết tủa trắng xuất hiện.
Bạn có biết
- Phản ứng trên được gọi là phản ứng đốt cháy.
- Nếu thiếu oxi, phản ứng cháy của propan xảy ra không hoàn toàn: sản phẩm cháy ngoài CO2, H2O còn có C, CO...
- Khi đốt cháy propan, số mol H2O thu được sau phản ứng luôn lớn hơn số mol CO2.
- Tương tự propan các ankan khác cũng tham gia phản ứng đốt cháy tương tự.

Ví dụ minh họa
Ví dụ 1: Một hỗn hợp X gồm etan và propan. Đốt cháy 16,2 g hỗn hợp X ta thu được CO2 và hơi H2O theo tỉ lệ thể tích là 11:15. Thành phần phần trăm theo thể tích của propan là:
A. 55%
B. 81,48%
C. 75%
D. 80%
Hướng dẫn:
Đặt nC2H6 = x mol ; nC3H8 = y mol
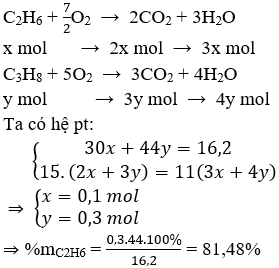
Đáp án B.
Ví dụ 2: Đốt cháy hoàn toàn m gam hỗn hợp gồm CH4, C2H6, C3H8 thu được 4,4 g CO2 và 3,6 g H2O. Tính giá trị của m.
A. 1g
B. 1,2g
C. 1,4g
D. 1,6g
Hướng dẫn:
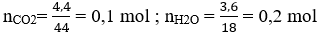
Ta có:
nC = nCO2 = 0,1 mol ⇒ mC = 0,1.12 = 1,2g
nH = 2.nH2O = 2.0,2 = 0,4 mol ⇒ mH = 0,4.1 = 0,4g
⇒ mankan = mC + mH = 1,2 + 0,4 = 1,6g
Đáp án D.
Ví dụ 3: Đốt cháy một hỗn hợp gồm 2 hidrocacbon A,B ( có M hơn kém nhau 28) thì thu được 0,3 mol CO2 và 0,5 mol H2O. Tìm CTPT của A và B.
A. CH4 và C2H6
B. C2H6 và C3H8
C. CH4 và C3H8
D. C2H6 và C4H10
Hướng dẫn:
Hydrocacbon A, B có M hơn kém nhau 28g → A, B thuộc cùng dãy đồng đẳng.
A, B + O2 → CO2 + H2O

Đáp án C.

