4C4H11N + 27O2
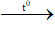 16CO2 + 22H2O + 2N2 - Cân bằng phương trình hoá học
16CO2 + 22H2O + 2N2 - Cân bằng phương trình hoá học
Phản ứng hoá học:
4C4H11N + 27O2
Điều kiện phản ứng
- Đốt cháy.
Cách thực hiện phản ứng
- Đốt cháy butylamin trong không khí, sau phản ứng thu được khí CO2, N2 và hơi nước.
Hiện tượng nhận biết phản ứng
- Sản phẩm sinh ra làm vần đục nước vôi trong.
Bạn có biết
- Tương tự butylamin, các amin khi bị đốt đều cháy và tỏa nhiều nhiệt.
- Khi đốt cháy butylamin, số mol H2O thu được sau phản ứng luôn lớn hơn số mol CO2.

Ví dụ minh họa
Ví dụ 1: Khi đốt cháy butylamin thu được H2O và CO2 với tỷ lệ số mol là
A. > 1. B. < 1.
C. = 1. D. không xác định được.
Hướng dẫn:
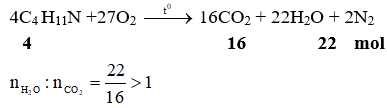
Đáp án: A
Ví dụ 2: Nhận định nào sau đây là sai?
A. đietylamin khi bị đốt cháy và tỏa nhiều nhiệt.
B. Đốt cháy butylamin, sau phản ứng thu được khí CO2 và hơi nước.
C. đốt cháy etylamin, số mol H2O thu được luôn lớn hơn số mol CO2.
D. Khi đốt cháy hoàn toàn metylamin, sản phẩm thu được làm đục nước vôi trong.
Hướng dẫn: Đốt cháy butylamin, sau phản ứng thu được khí CO2, N2 và hơi nước.
Đáp án: B
Ví dụ 3: Đốt cháy 1 mol khí butylamin trong không khí, sau phản ứng thu được khí CO2 và N2 có tổng số mol là
A. 4,5. B. 2.
C. 1,5. D. 2,5.
Hướng dẫn:
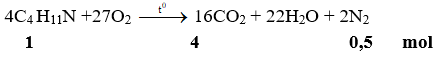
Đáp án: A

