KOH + CH3COOH → CH3COOK + H2O - Cân bằng phương trình hoá học
Phản ứng hoá học:
KOH + CH3COOH → CH3COOK + H2O
Điều kiện phản ứng
- Phản ứng xảy ra ngay điều kiện thường.
Cách thực hiện phản ứng
- Nhỏ từ từ KOH vào ống nghiệm chứa CH3COOH và một mẩu quỳ tím.
Hiện tượng nhận biết phản ứng
- Ban đầu mẩu quỳ có màu đỏ, sau khi nhỏ KOH mẩu quỳ mất màu đỏ, dư KOH mẩu quỳ chuyển sang màu xanh.
Bạn có biết
- Các axit hữu cơ khác như HCOOH, C2H5COOH… cũng phản ứng với KOH tương tự axit axetic.
- Phản ứng giữa KOH và CH3COOH là phản ứng trung hòa.

Ví dụ minh họa
Ví dụ 1:
Cho 0,1 mol KOH phản ứng vừa đủ với 100ml CH3COOH aM. Giá trị của a là
A. 0,1. B. 0,01. C. 0,05. D. 1.
Hướng dẫn giải
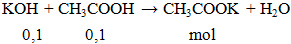
a = 0,1 : 0,1 = 1M.
Đáp án D.
Ví dụ 2:
Phản ứng nào sau đây là phản ứng trung hòa?
A. 2KOH + CO2 → K2CO3 + H2O
B. KOH + SO2 → KHSO3
C. KOH + CH3COOH → CH3COOK + H2O
D. 2KOH + CuSO4 → K2SO4 + Cu(OH)2
Hướng dẫn giải
Phản ứng trung hòa là phản ứng KOH + CH3COOH → CH3COOK + H2O
Đáp án C.
Ví dụ 3:
Cho 100ml CH3COOH 0,1M phản ứng vừa đủ với dung dịch KOH thu được dung dịch X. Khối lượng muối tan có trong dung dịch X là
A. 0,745g. B. 0,98g. C. 0,754g. D. 1,10g.
Hướng dẫn giải
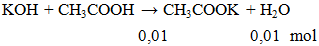
mmuối = 0,01.98 = 0,98 gam.
Đáp án B.

